🔳EPR効果(enhanced permeabilited and retention effect)とDDS(ドラッグデリバリーシステム)
■主ながんの原因
①化学物質、②放射線、③慢性感染(による炎症)の3つ。
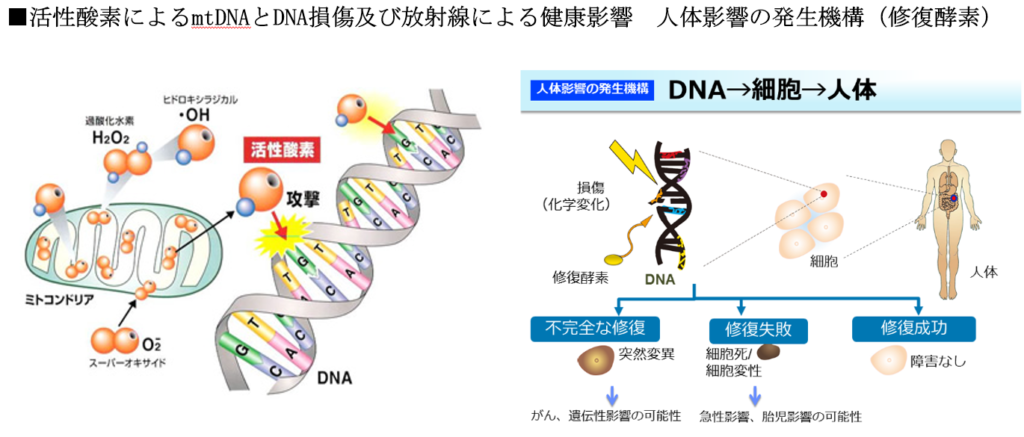
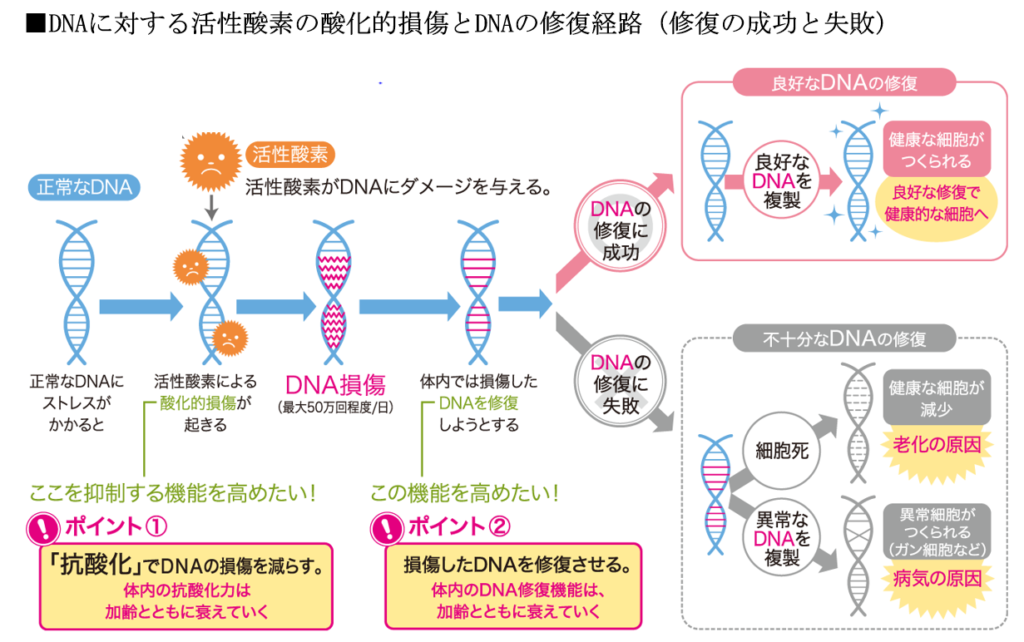
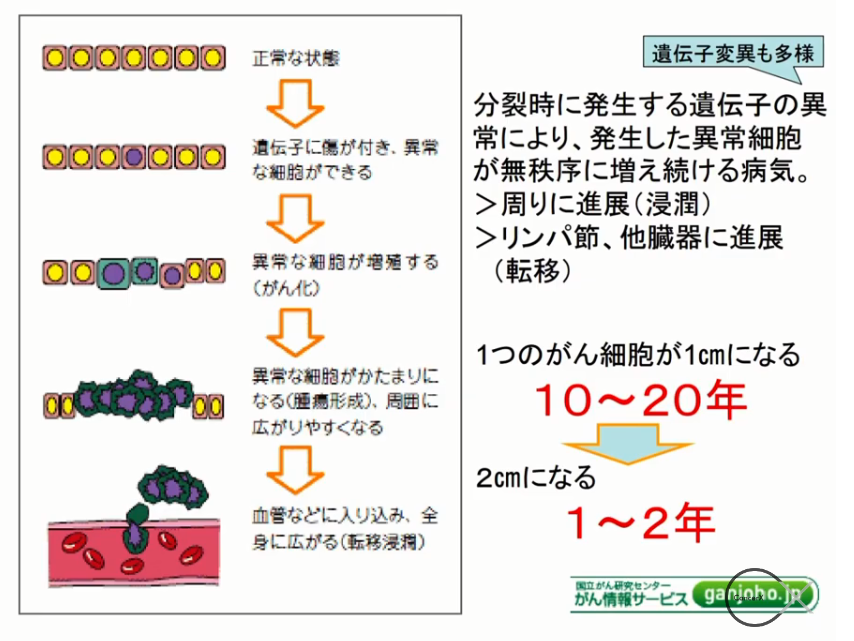
いずれも活性酸素が発生して、DNAを傷つけ、正常細胞が突然変異を起こしがん細胞になる。
活性酸素を消去する抗酸化酵素(SOD、グルタチオン、タカラーゼ等)は加齢と共に衰え、活性酸素の処理が追い付かなくなる。
一方、損傷したDNAを修復する機能も加齢と共に衰える。
◆ヒトの腫瘍
⇒当初の炎症から10年以上30年もかかって、癌に進展したと考えらるものが多い。(例:肝癌、すい癌、胆のう癌、胃癌、大腸癌等)
⇒その間、病巣では炎症反と類似の反応。
⇒例えばスーパーオキサイド(O₂⁻・)と一酸化窒素(NO)が炎症局所で同時に生成・反応し、活性酸素であるパーオキシナイトライト(過酸化亜硝酸、ONOO⁻)を生成。
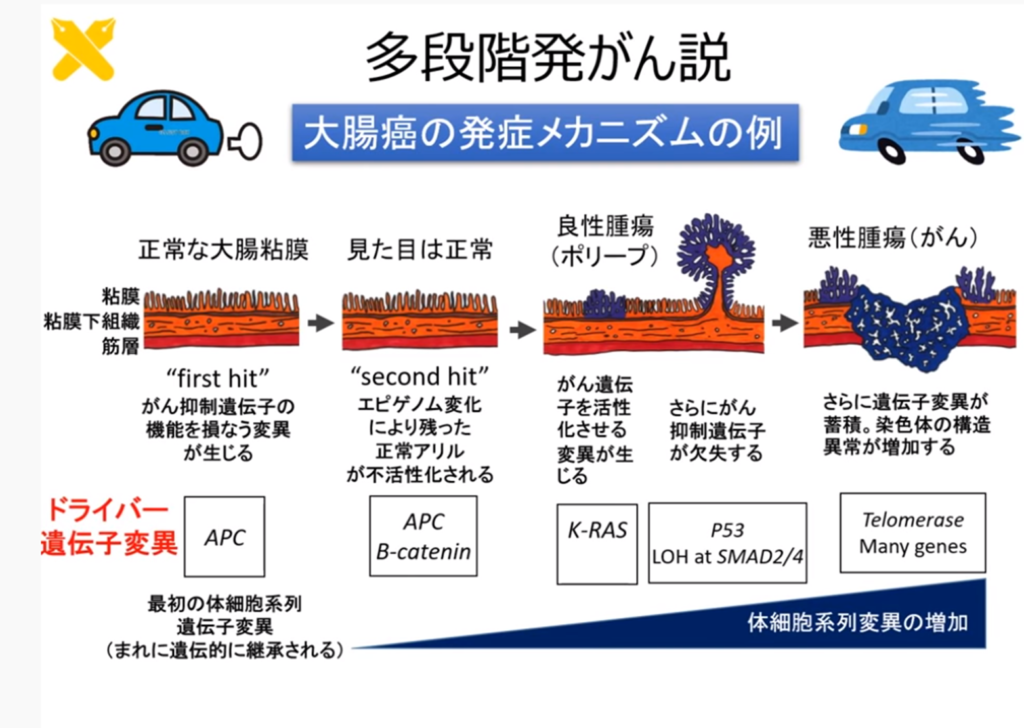
⇒それらは変異原となる。その結果、その遺伝子変異の多さは驚くべき数になる。
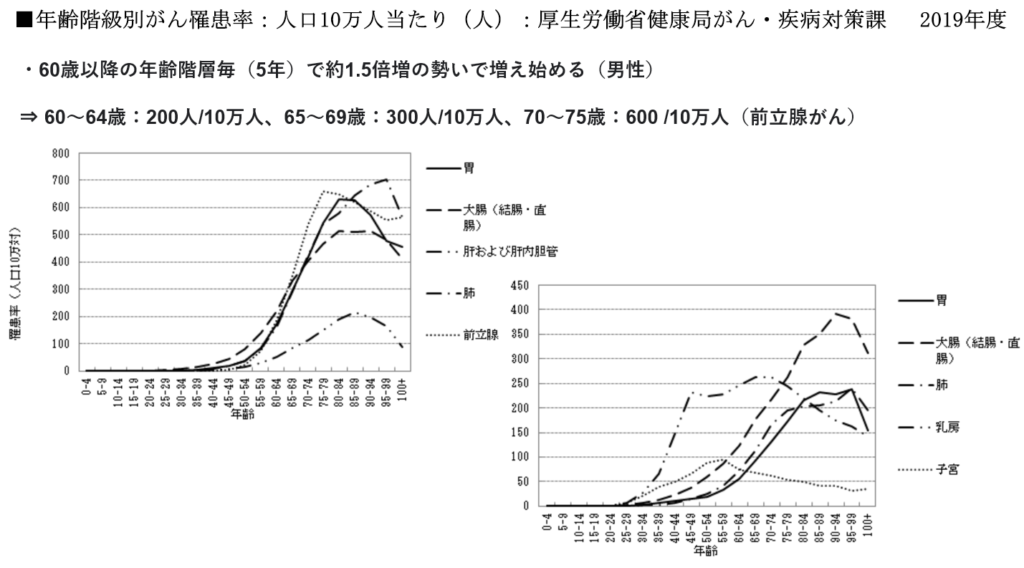
◆年齢階層別がん罹患率の推移
・男性は55歳以上の年齢に達すると、急激に罹患率のカーブが立ち上がる。
⇒『抗酸化酵素』と『損傷したDNA修復機能』が加齢と共に衰える要因は無視できない。
■がん化学療法剤の動向
◆制癌剤の承認評価基準
・延命率の延長が中心
⇒ほんのわずか2~3ヵ月の延長が大半。
⇒腫瘍の縮小の評価も50%以上縮小を有効とし、その持続期間はほんの短期間の場合が多い。
⇒腫瘍マーカー(表1)の低下も評価の中心。
⇒患者にとって極めて大切なQOLの改善(表1)の評価は中心的な課題になっていない。

◆正常細胞にも悪影響(副作用)を与える癌化学療法剤
・多くの制癌剤は低分子
⇒全身に均一か、がん組織よりも正常組織の方に薬剤が集まる。
⇒副作用が起き、患者のQOLの向上に繋がらない。

上記の内容は、故前田 浩氏の発表資料「高分子薬剤の切り拓くNew Dimension─副作用のない固型癌に普遍的な制癌剤は可能だ─(1)」より転記
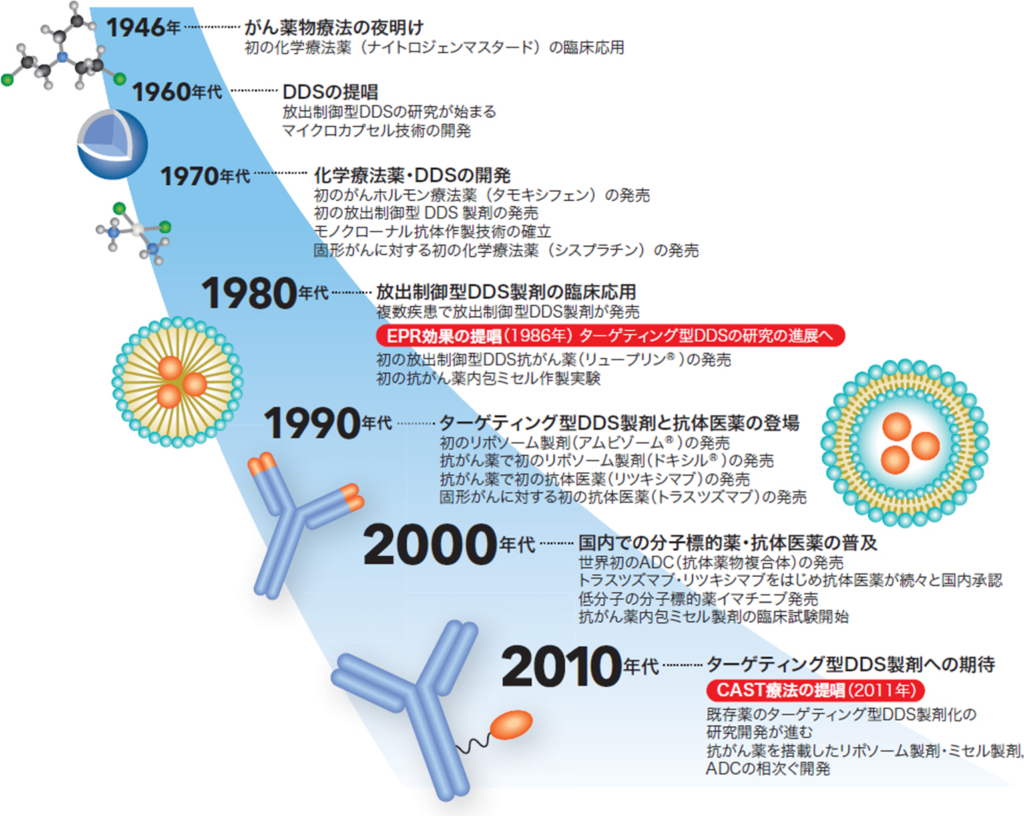
■がん薬物療法を加速させるDDSの研究変遷
・1946年に初の化学療法が登場
⇒1986年にEPR効果の論文が故前田 浩(前熊本大学名誉教授)と松村 保広(前国立がん研究センター先端医療開発センター新薬開発分野分野長)より発表された。
(注)副作用のない抗ガン剤の研究でノーベル化学賞候補に(2016年):同論文が2016年、トムソン・ロイター引用栄誉賞を受賞(18年8月時点で被引用回数5500回以上)。
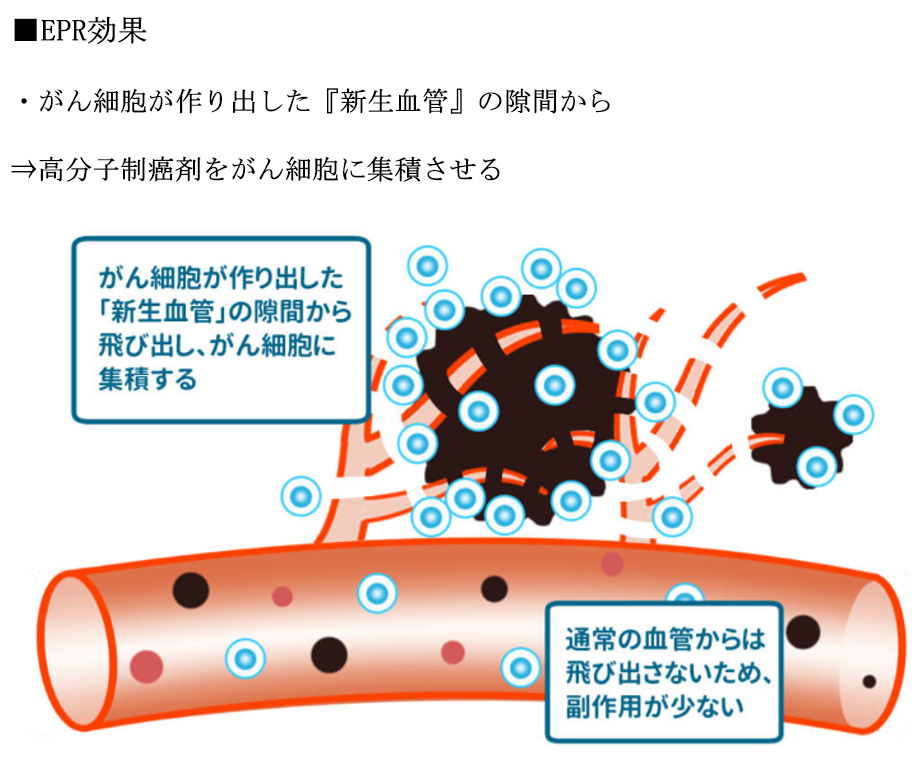
<参考情報>
・がんの弱点とは?癌の成長・転移に必要な血管新生を阻害する食べ物3つ
(がん情報チャンネル・外科医 佐藤のりひろ氏のYouTube動画より)
・血管新生の仕組みの説明
・がん細胞の血管新生を抑える食品3つ
⇒大豆、にんにく、ベリー類を紹介。
・1986年以後
⇒ターゲティング型のDDSに着目した医薬品開発の道が開けた。
⇒近年、DDS製剤の開発が本格化している。
上記内容は松村氏の下図の説明より転記
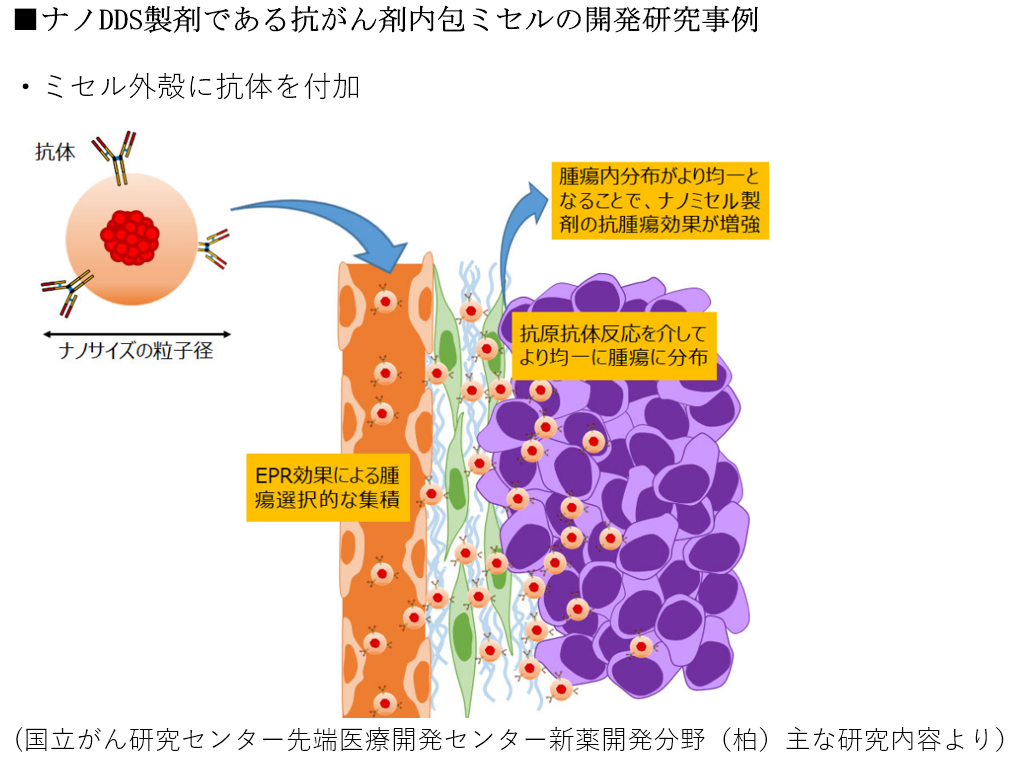
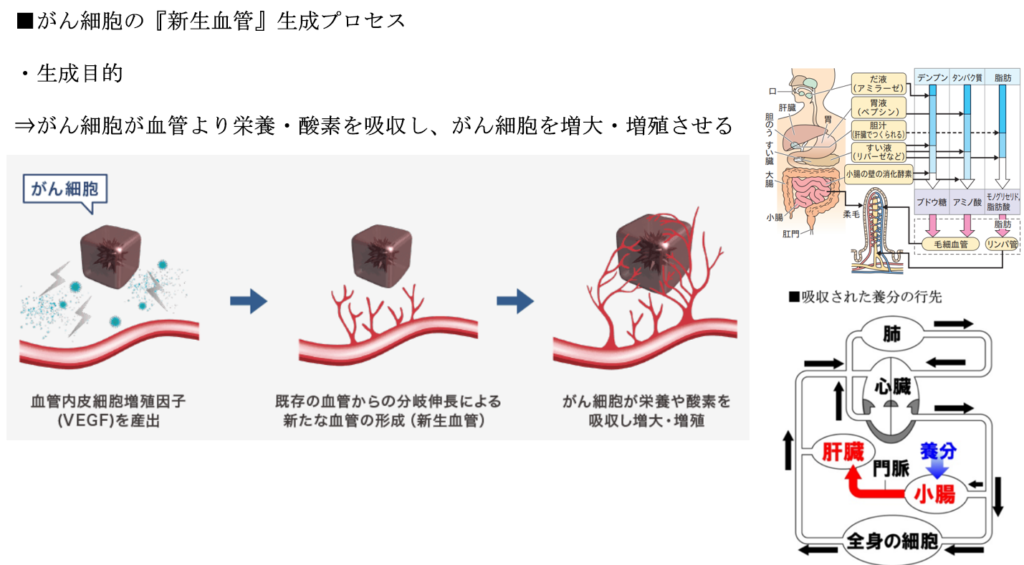
■がん細胞周辺で見られる現象
◆がん細胞周辺の血管
・不完全で
⇒正常な血管では通過できない大きな分子(=高分子、数百㎚:ナノメートル)でも貫通して
⇒がん組織周辺に集積(浸透)できる。
⇒がん組織だけに大きな分子(高分子抗がん剤)を届ける事ができる。
⇒がん細胞周辺に医薬品を選択的にデリバリーするDDS(ドラッグデリバリーシステム)として機能。
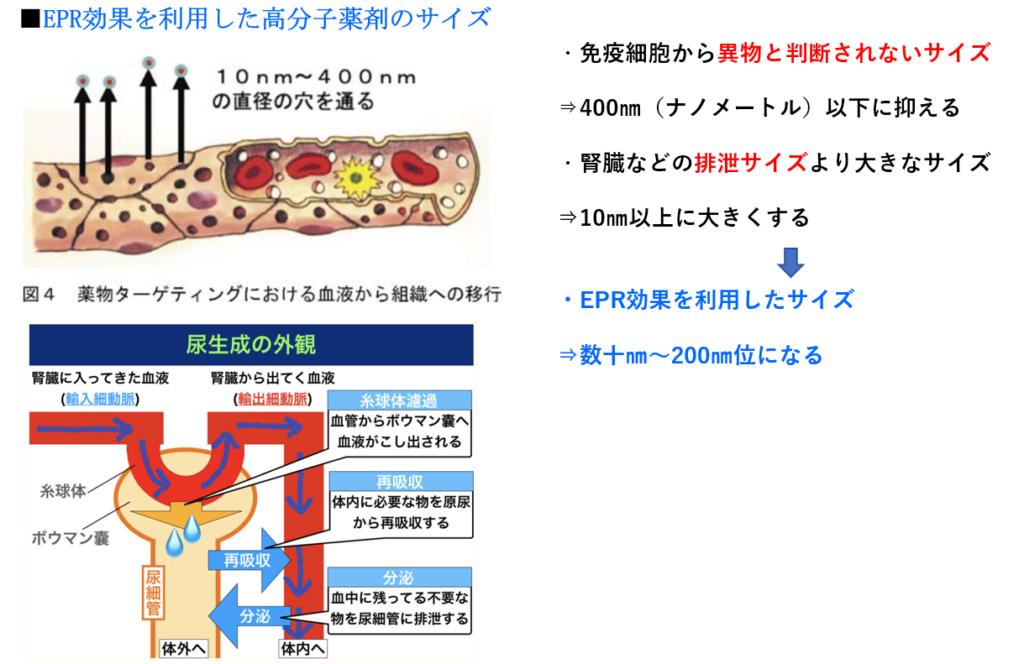
左下図)https://evidencenote.com/7500221-2/

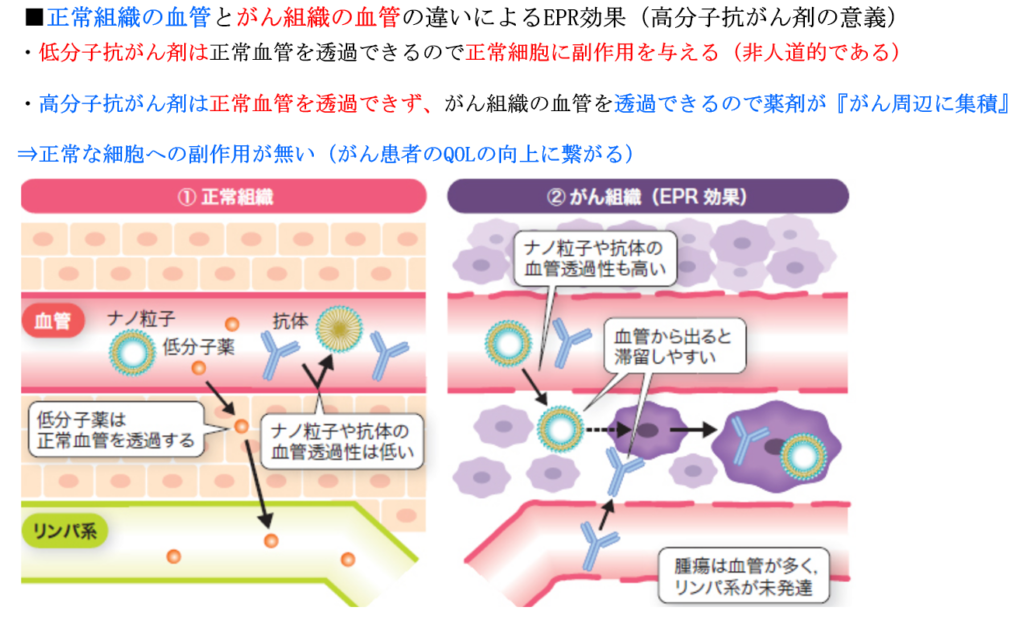
◆固型癌組織&正常組織の特徴及びDDSに適した高分子抗がん剤の意義
【固型癌組織】
●腫瘍特異現象(ⅰ)
血管の壁は、正常な組織と異なり、数10㎚~200㎚程の比較的に、大きな隙間がたくさんある。
・血管の構造
⇒粗雑。
⇒低分子はもちろん高分子物資までも容易に漏出し
⇒リンパ系(高分子や脂肪球を除去するための下水路系に相当)の機能不全の為
⇒いったん組織中に漏出した高分子物質の場合、それがそこに長期間にわたり未回収のまま残留する事を1986年発見し、これをEPR効果と命名した。
・10㎚以上のサイズの微粒子は、正常組織へは到着せず
⇒がん組織が作った粗雑な血管から腫瘍組織だけに高分子物資が届く。
・副作用の回避(DDSに適した高分子抗がん剤)
⇒高分子抗がん剤は正常組織に薬が入らないので副作用が回避できる。
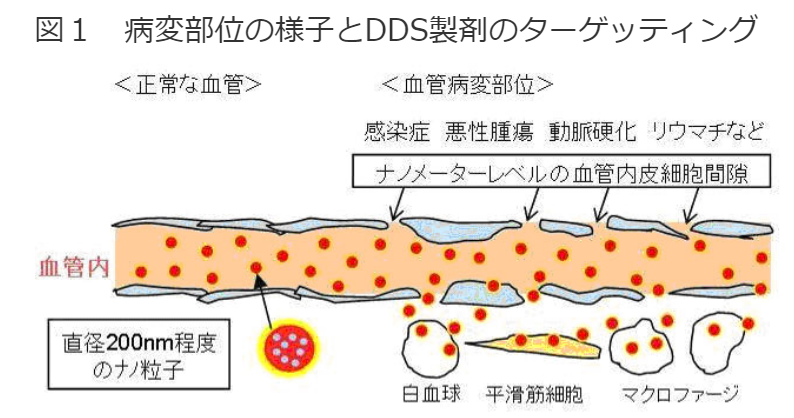
・免疫細胞からの攻撃も回避
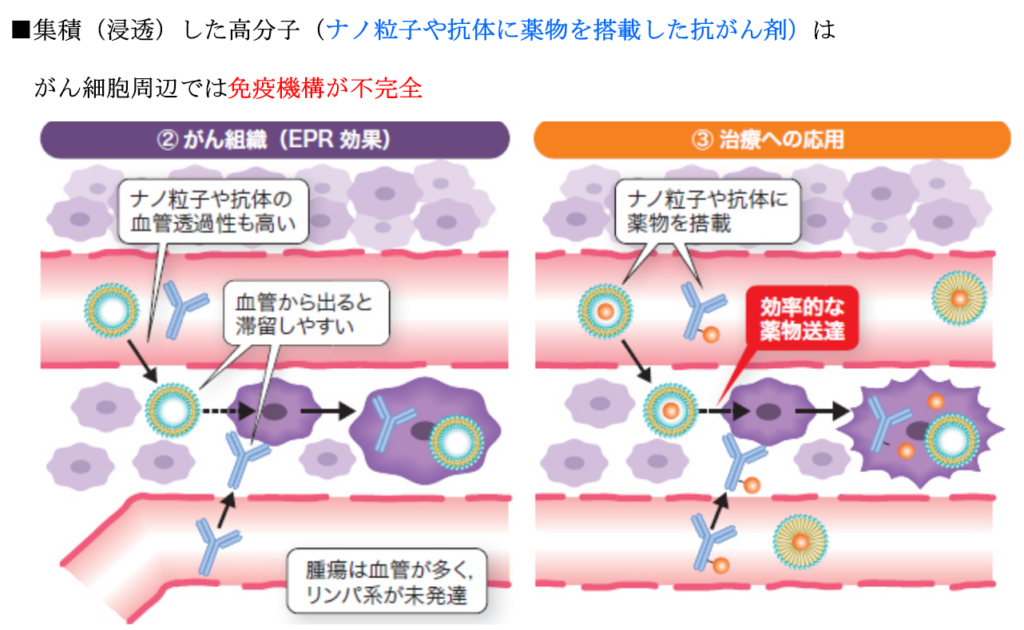
⇒集積(浸透)した高分子はがん細胞周辺では免疫機構が不完全
⇒免疫細胞による異物排除が正常に行われない為に高分子が保持(retention)される。
【正常組織】
・血管のつくり方
⇒血管の壁は5㎚程(1㎚は百万分の1mm)の極小の隙間が規則正しく並んでいる。
・EPR効果は見られず。
⇒高分子薬物の蓄積がないので毒性も発現しない。
⇒万一そこにデリバリーされても、リンパ系が回収除去されるわけである。
注)上記内容は故前田 浩氏の発表資料『癌研究における分子生物学パラダイムの苦悩40年にわたる苦戦の経験から原点回帰へ』よりの転記
■EPR効果の概要を知るために、故前田 浩氏が投稿された記事を中心に紹介する。
・発表資料:高分子薬剤の切り拓くNew Dimension
─副作用のない固型癌に普遍的な制癌剤は可能だ─(1)から(4)
https://www.jst.go.jp/tt/journal/journal_contents/2018/04/1804-07_article.html
◆EPR効果(高分子薬剤を届ける)の増強法
・低分子化合物薬剤の弊害
⇒静脈内に投与すると全身の毛細血管から全身の組織に浸透し(自由拡散)
⇒もともと毒性のあるほとんどの制癌剤は
⇒正常な組織にくまなく浸透し、毒漬け状態になり、副作用となる。
⇒しばしば毒物(制癌剤)の到達は癌組織の方が少ない。
・癌組織に栄養素を供給している腫瘍の栄養血管(動脈)
⇒心筋梗塞と同様に、血栓とかフィブリン凝固系の亢進により
⇒血流がほとんど無いか、乏しくなっており
⇒薬物である制癌剤は健常組織よりも少なめにしか届かない。
・血管拡張剤による血栓の消去
⇒ニトログリセリン等で腫瘍の栄養血管に薬物を届けられる事を発見した。
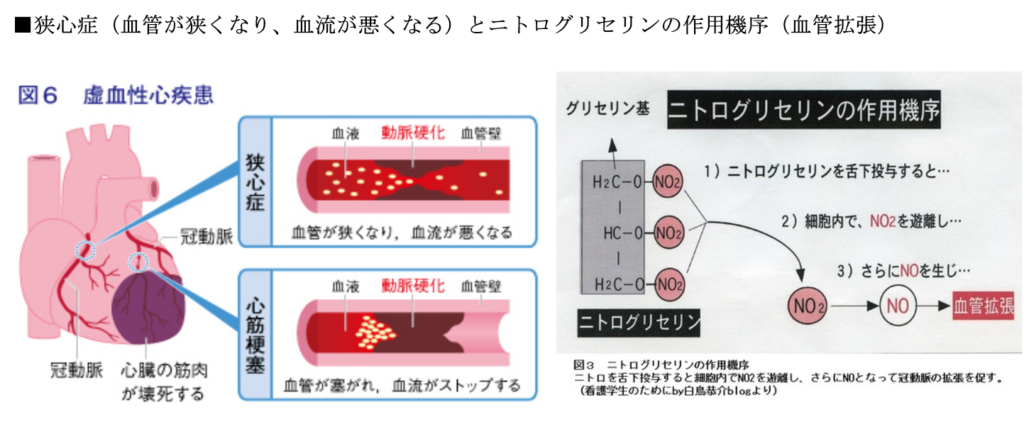
・EPR効果の増強剤
⇒ニトログリセリンやACE阻害剤(エナラプリル等)は安全な薬物で、
⇒容易に制癌剤の腫瘍デリバリーを2から3倍も上げる事ができる。

■「がん免疫療法」の観点から比較(故前田 浩氏の発表資料とは関係が無い)
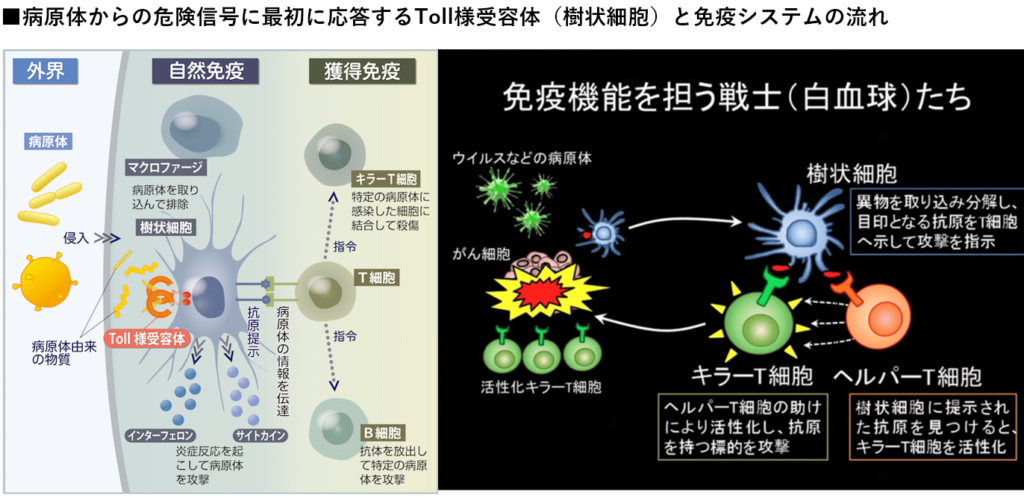
◆ウイルス等の異物が体内にいるかをパトロールする樹状細胞と異物を攻撃するT細胞
・樹状細胞
⇒ウイルス等の異物を取込み、分解し、抗原をヘルパーT細胞に提示
・ヘルパーT細胞
⇒抗原を見つけるとキラーT細胞を活性化(抗原を連絡する)させる。
・キラーT細胞
⇒抗原を持つ標的(ウイルス等)を攻撃し、がん細胞を破壊する。
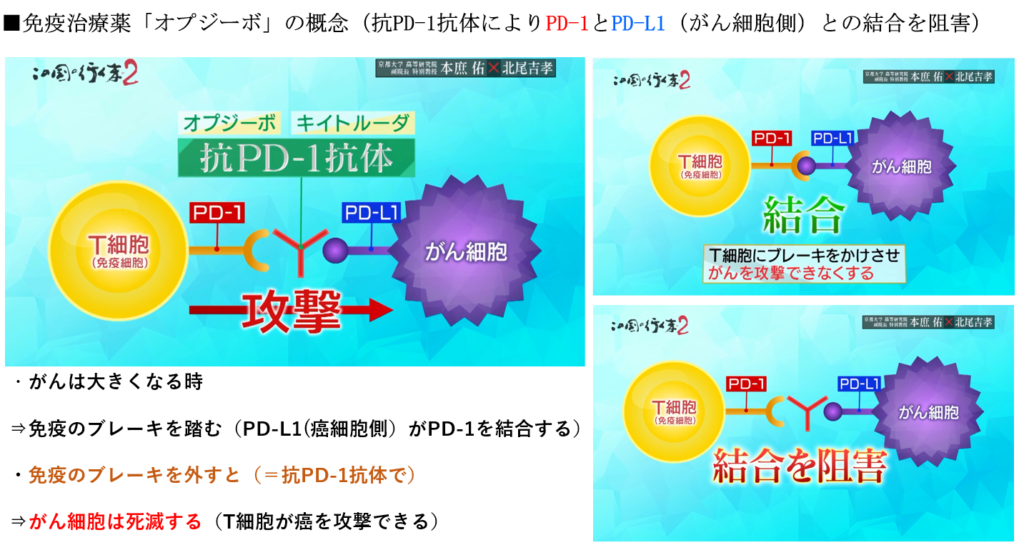
・がん細胞の巧妙さ
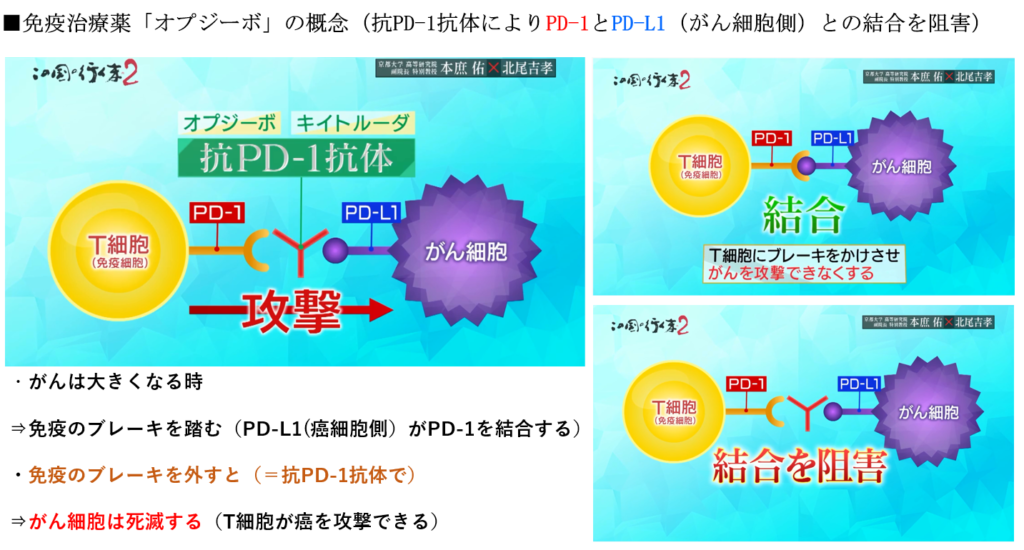
⇒がん細胞は免疫のブレーキ(PD-L1)を獲得しており
⇒ブレーキが掛かる(PD-L1とPD-1の結合)と
⇒キラーT細胞はがん細胞を攻撃できない。

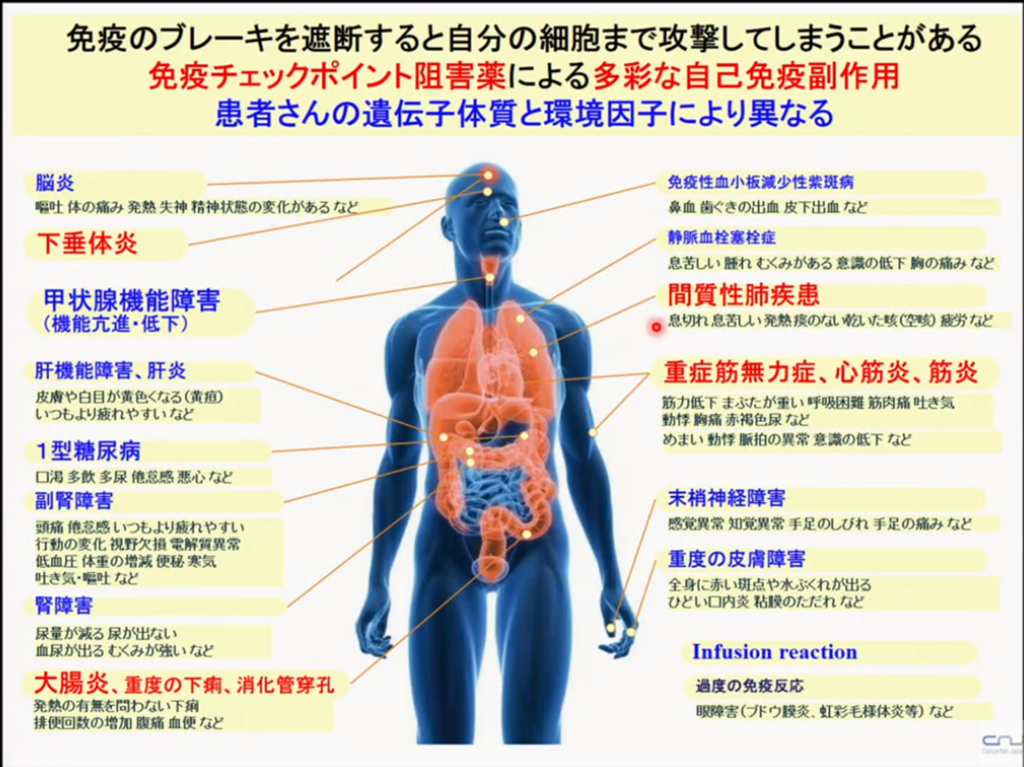
◆免疫チェックポイント阻害剤(PD-1抗体:オプジーボ)
・PD-1抗体を挿入すると
⇒PD-L1のブレーキが外れ
⇒キラーT細胞が活性化(攻撃する)される。
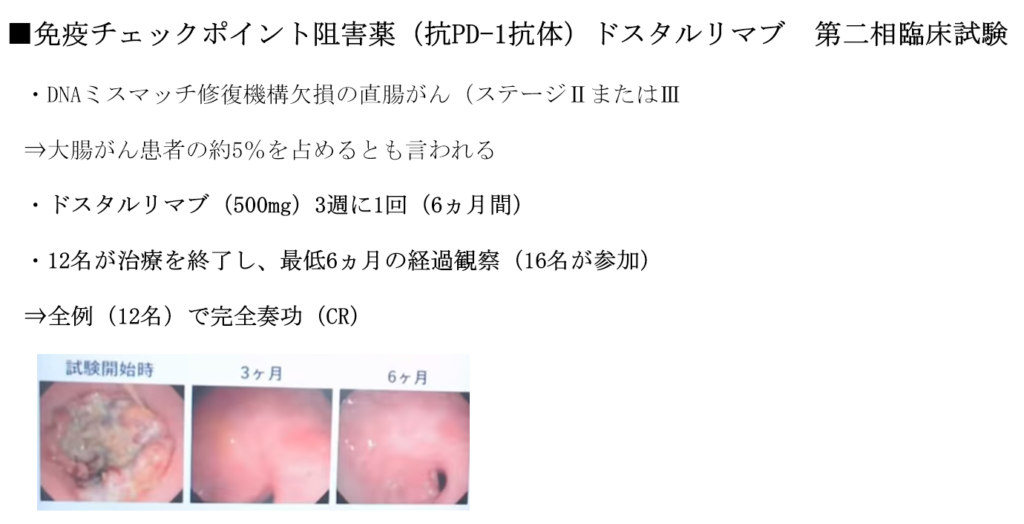
❖免疫チェックポイント阻害剤の新薬開発事例
【衝撃!】新薬で進行した直腸がんが消えた?抗PD-1抗体(免疫チェックポイント阻害薬)ドスタルリマブの臨床試験
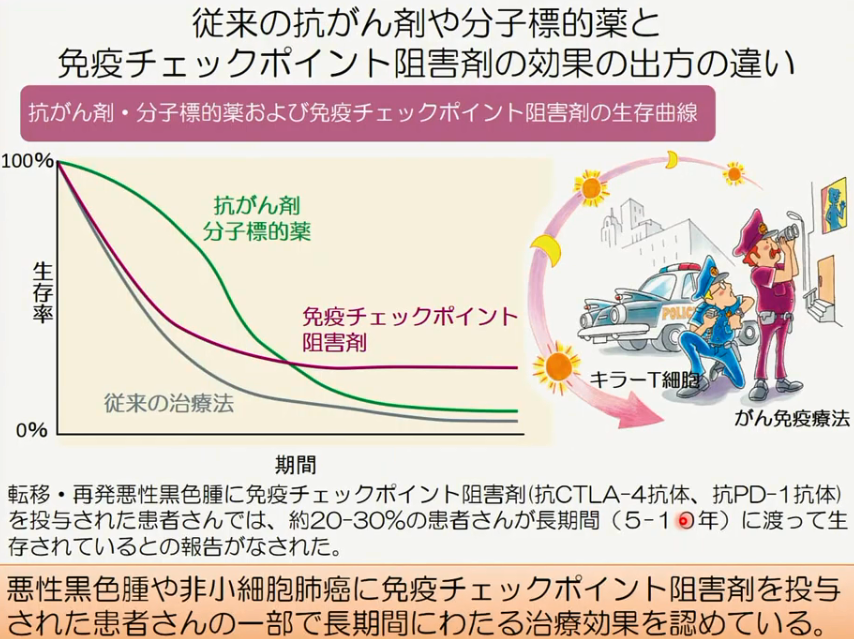
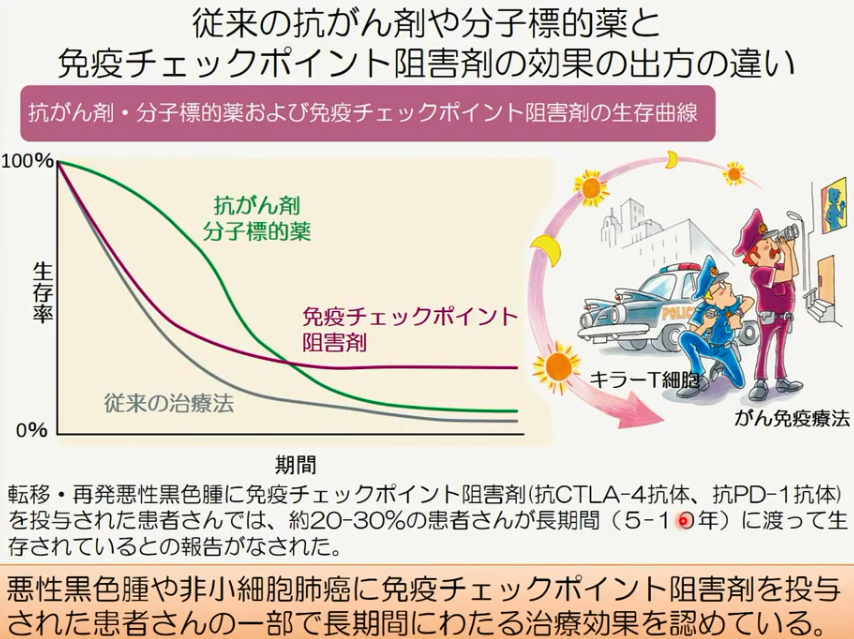
■従来型の抗がん剤や分子標的薬と免疫チェックポイント阻害剤の効果の出方の違い
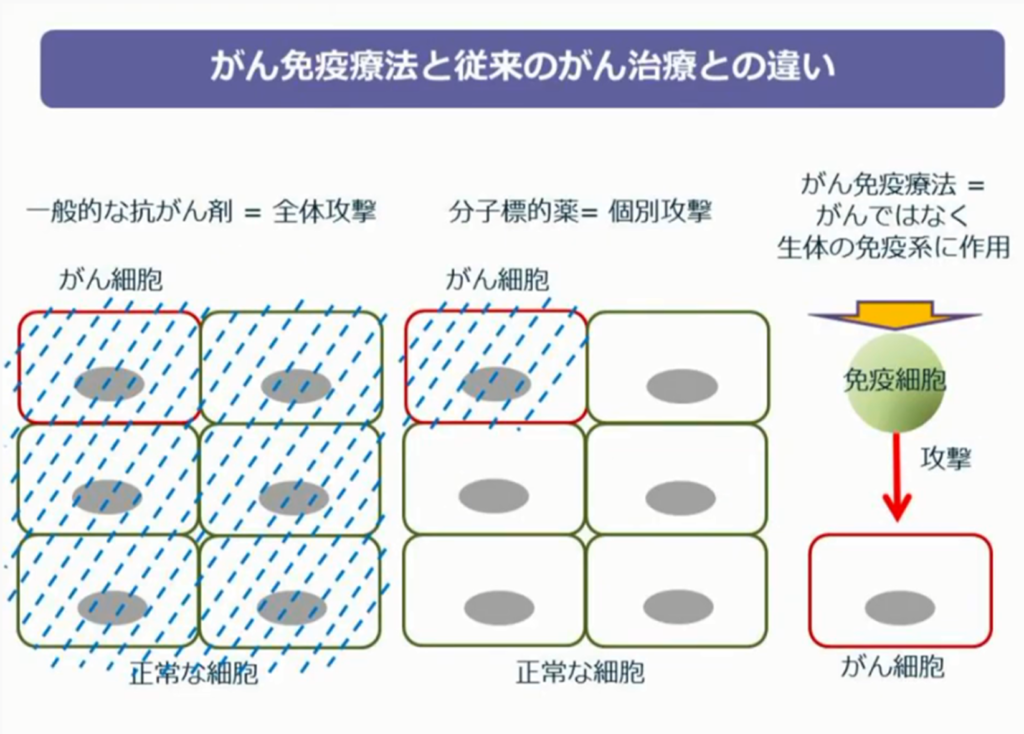
◆免疫の二面性:自己免疫疾患(免疫の暴走=サイトカインストーム)
・本来守るべき自身の正常な細胞や組織を『異物』として認識し、攻撃する事で病気を発症させる。
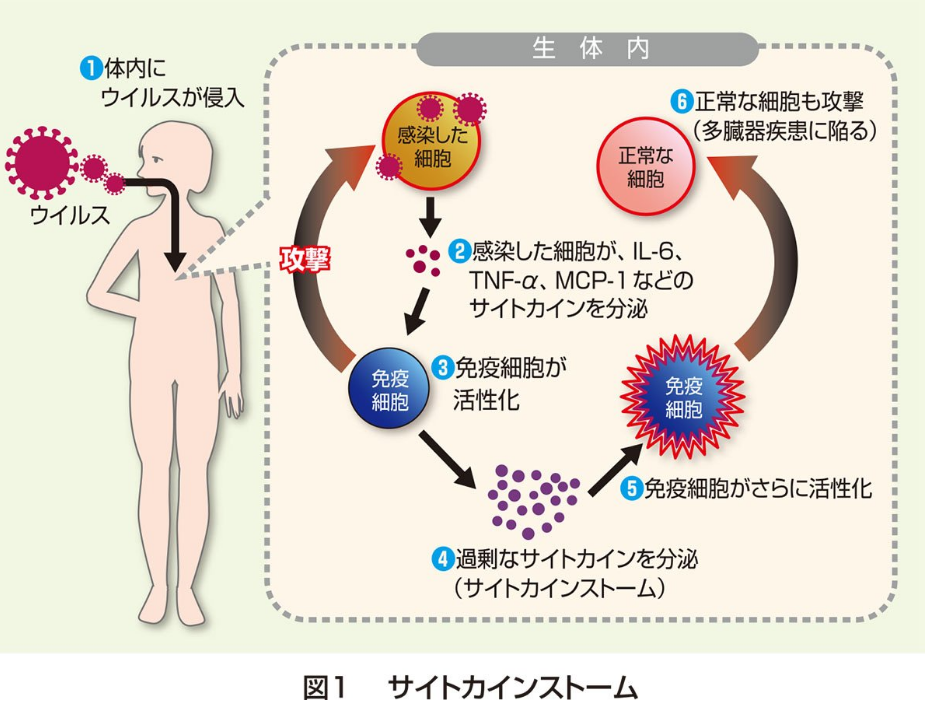
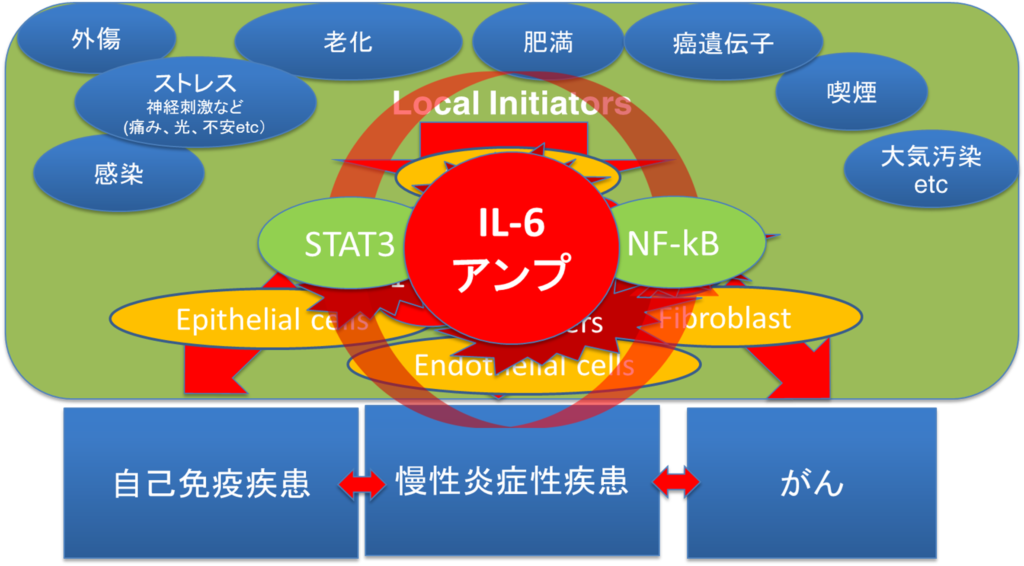
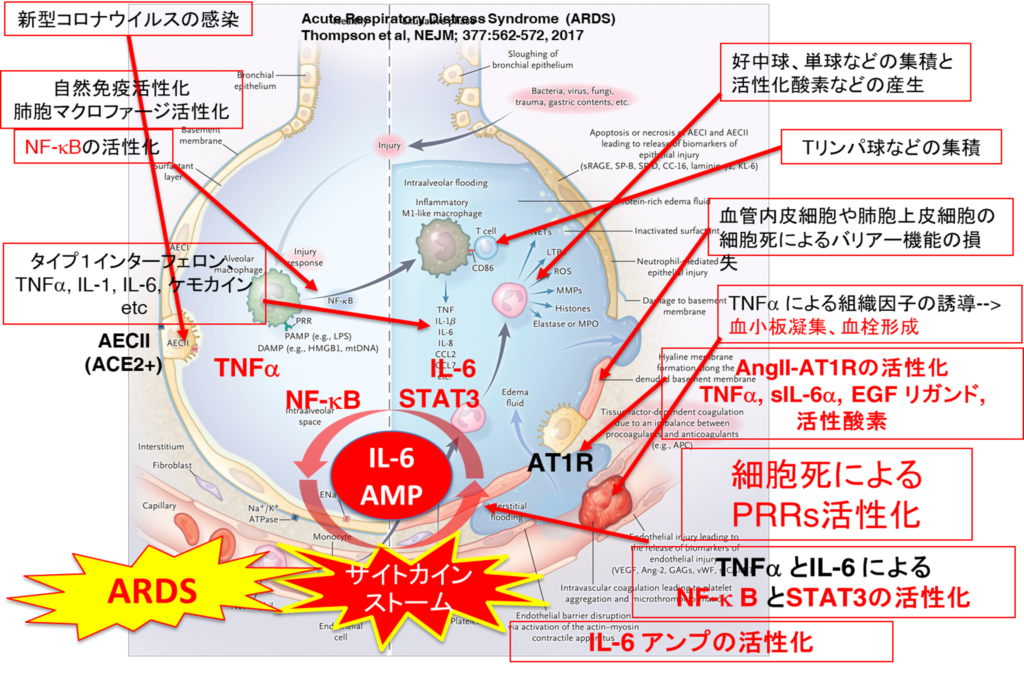
・IL-6AMP(IL-6アンプ)
⇒慢性炎症誘導の基盤として炎症性サイトカイン産生増幅回路
⇒免疫反応がウイルスを排除できない間に、ウイルス感染により肺胞上皮細胞などの細胞死が生じる。
⇒大量の死細胞から放出されたダメージ関連分子パターン(DAMP:Damage associated molecular pattern)がPRRsに認識されNF-kBが活性化される。
⇒その結果IL-1b、TNFαやIL-6などのサイトカインやケモカイン産生が誘導され、
⇒IL-6アンプが活性化されると考えられる。
注)ARDS:Acute Respiratory Distress Syndrome=急性呼吸促迫症候群(新型コロナウイルス等の重症患者で見られた症状で致死率が高い)
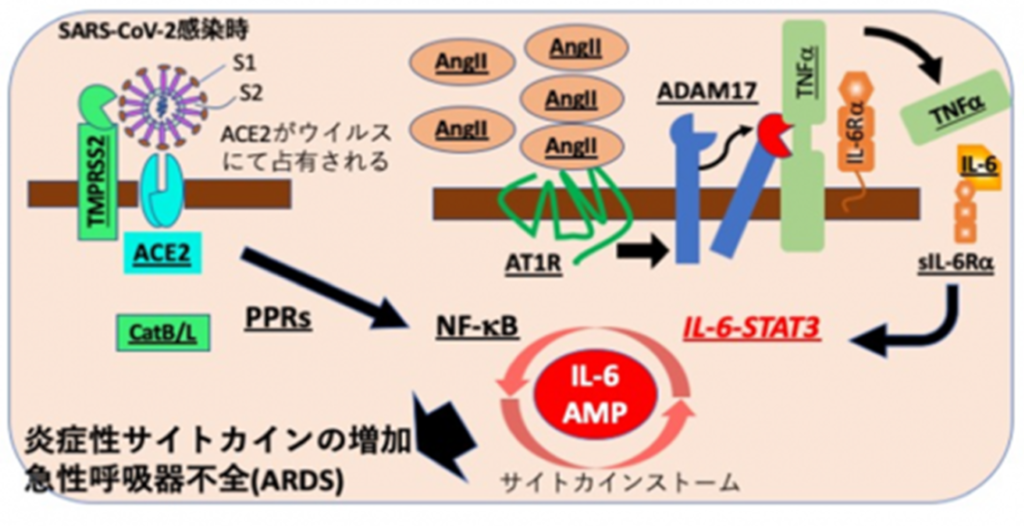
平野 俊夫(国立研究開発法人 量子科学技術研究開発機構 理事長、前 大阪大学 総長) https://www.youtube.com/watch?v=A-cs-PddxU4
◆抗IL-6受容体抗体トシリズマブ(=商品名:アクテムラ)
・関節リウマチ(自己免疫疾患)などの慢性炎症性疾患の治療に有効である
⇒IL-6などのサイトカインは抗ウイルス活性があるので、
⇒感染初期に投与すると逆効果になると考えられるので、
⇒投与時期は血中IL-6濃度やD-ダイマーなどの組織損傷マーカーなどを指標に慎重に選ぶ必要がある。
これらの阻害剤はウイルスや細菌のみならず外傷などで引き起こされるサイトカインストームが原因のARDSはもちろんのこと腎機能不全など他の臓器不全にも効果が期待できる。

上記内容は平野 俊夫氏の発表資料「新型コロナウイルス感染症(COVID-19)はサイトカインストーム症候群である」より一部抜粋して転記。
尚、抗IL-6受容体抗体トシリズマブ(=商品名アクテムラ:2008年4月 厚生労働省の認可を受ける)は新型コロナウイルス重症患者(サイトカインストームに直面した患者)に投与され、生命回復効果もあったとの事。

以下、故前田 浩氏の発表資料:高分子薬剤の切り拓くNew Dimension
─副作用のない固型癌に普遍的な制癌剤は可能だ─(1)から(4)の内容を転記
■「マウスの癌とヒトの臨床での癌との違い」及び「EPR効果の増強による腫瘍デリバリーの増強」
◆マウスの癌
・大きさは均一、年齢は若い、遺伝子系統は同一系。
⇒上記のように均一な背景では生物統計学は有効である。
◆ヒトの癌
・マウスの実験腫瘍のように均一でなく、おびただしいバラツキがある。
・大きな腫瘍になると組織のかなりの部分は壊死しており、血管もないか、血栓を形成している。
・血管の組織(腫瘍部)では阻血になっており、血流もないか、あるいは乏しいものが多い。
・血流は同じ肝臓にできた腫瘍でも、原発性肝癌と他の臓器からの転移性肝癌では
⇒前者は血流が豊富であるが、後者は乏しく、全く異なる血流動態である。
このような背景では厳密な統計学は適用できないと言われている。

・ヒトの腫瘍
⇒当初の炎症から10年以上30年もかかって、癌に進展したと考えらるものが多い。(例:肝癌、すい癌、胆のう癌、胃癌、大腸癌等)
⇒その間、病巣では炎症反と類似の反応、
⇒例えばスーパーオキサイド(O₂)と一酸化窒素(NO)が炎症局所で同時に生成・反応し、活性酸素であるパーオキシナイトライト(過酸化亜硝酸、ONOO⁻)を生成。
⇒それらは変異原となる。その結果、その遺伝子変異の多さは驚くべき数になる。
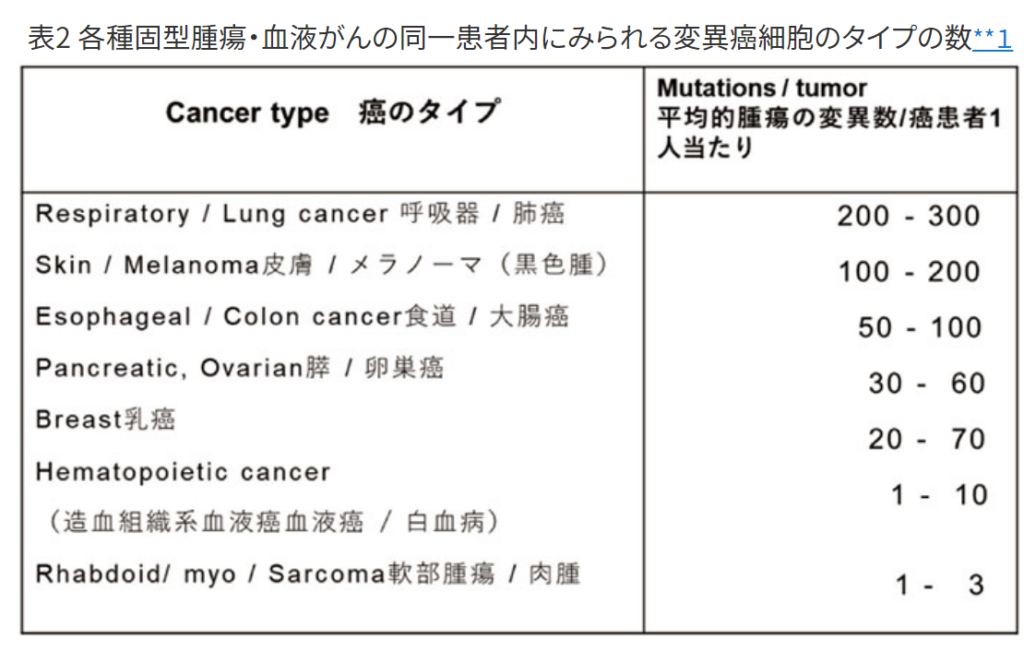
変異が多い固型癌に比較し、
血液癌(白血病)や軟部組織の腫瘍では、1~10種程度と少ない。
変異がなければ
グリベッグのような抗慢性白血病薬の特効薬があれば、著明に効果が見られる。(>奏功率90%)
この事実(固型癌は変異が多く、血液癌は変異が少ない)は
癌治療の原理としての標的分子や抗原エピトープを狙う分子標的薬や抗体医療の標的も
変わっている事を示し、
そのような対癌戦略は効果がないといえる。
◆EPR効果の増強による腫瘍デリバリーの増強
・固型腫瘍の血流
⇒血管の塞栓(そくせん)、腫瘍のマスの増大による血管の圧排などに起因して血流はしばしば不全になっている。
⇒この類似例としては狭心症で、心臓の冠状動脈の血流不全によるものである。
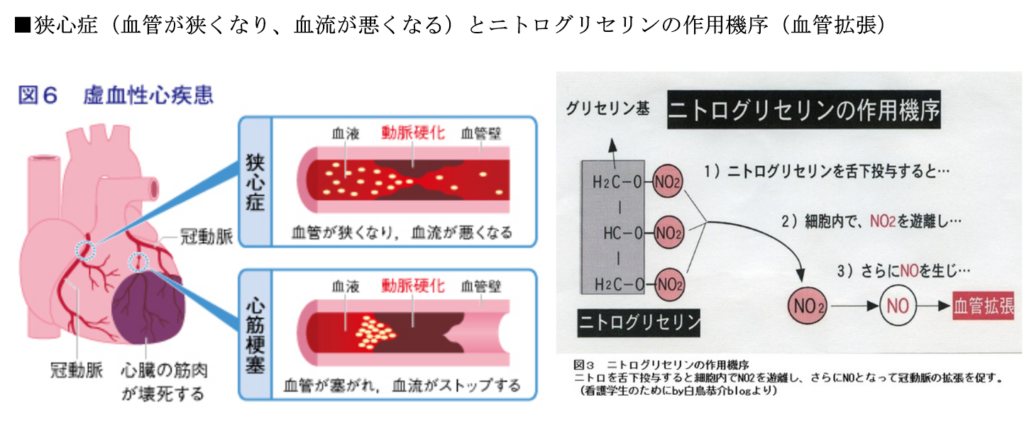
⇒その対策として、最もよく知られているのがニトロ剤の投与である。
⇒ニトログリセリンやニトロール(ISDN)等は経口/経皮投与で急速に血中に移行し、亜硝酸(NO₂⁻)イオンになる。
⇒虚血局所、腫瘍部などpO₂の低いところでは
⇒亜硝酸(NO₂⁻)は一酸化窒素(NO)に変換される。
⇒NOは血管拡張作用を発現し、血管拡張と同時に血管の透過性(EPR効果)の亢進をもたらす。
⇒更に、NOそのものも腫瘍の増殖に抑制的作用する。
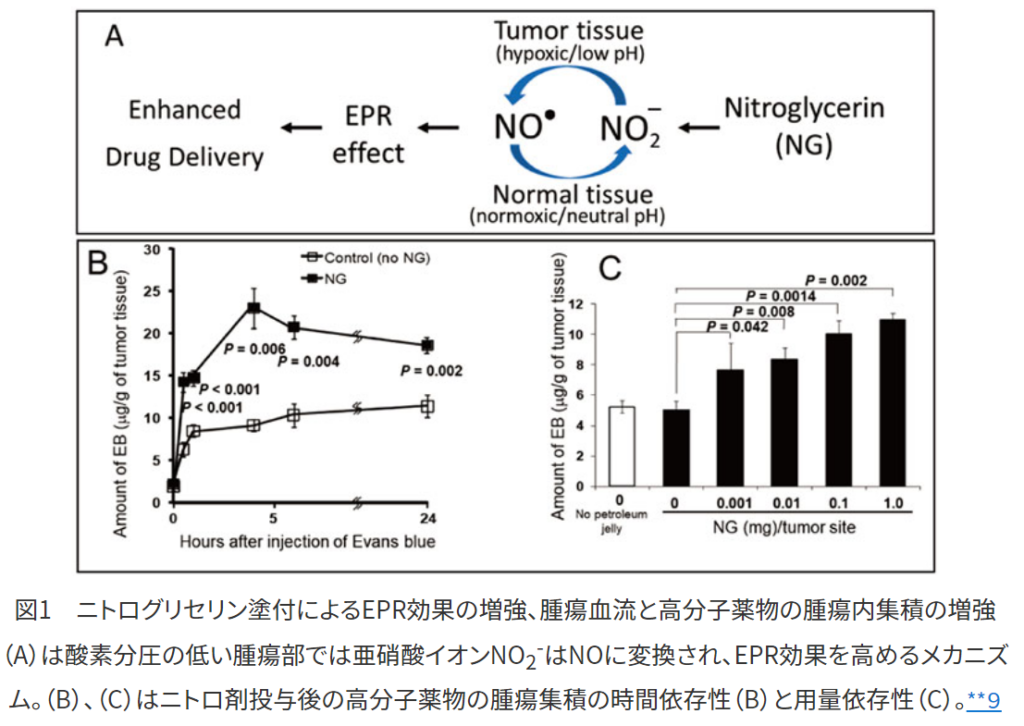
・EPR効果の増強によるデリバリー効果
⇒ニトログリセリンやACE阻害剤(エナラプリル等)は安全な薬物で、容易に制癌剤の腫瘍デリバリーを2から3倍も上げる事ができる。
⇒しかも、ニトロ剤は正常組織では作用しない(亜硝酸(NO₂⁻)から一酸化窒素(NO)に変換がない)ので、好都合。
⇒この手法を高分子化ピラルビシンのパイロットスタディに使用し、好成績を上げている。
・ニトロ剤の投与による稀に起きる事案
⇒低血圧のヒト(最高血圧が100以下)では
⇒血管拡張により、万一の血圧低下(ショック)の心配があるので、
⇒そのようなケースではACE(Angiotensin Ⅰ変換酵素)阻害剤を用いることにより可能になる。
◆自家発癌の乳癌のラットモデル実験
・腫瘍はDMBA(ジメチルベンズ[a]アントラセン)投与
⇒通常は径が5~6㎚(ナノメートル)の腫瘍に対して評価を行うが
⇒径が20~30mmになったものを、高度進行癌のモデルとして治療対象に選んだ。
・高分子型制癌剤単独投与群とニトロ剤併用群比較
⇒それぞれ4回投与で、投与後130日目での評価
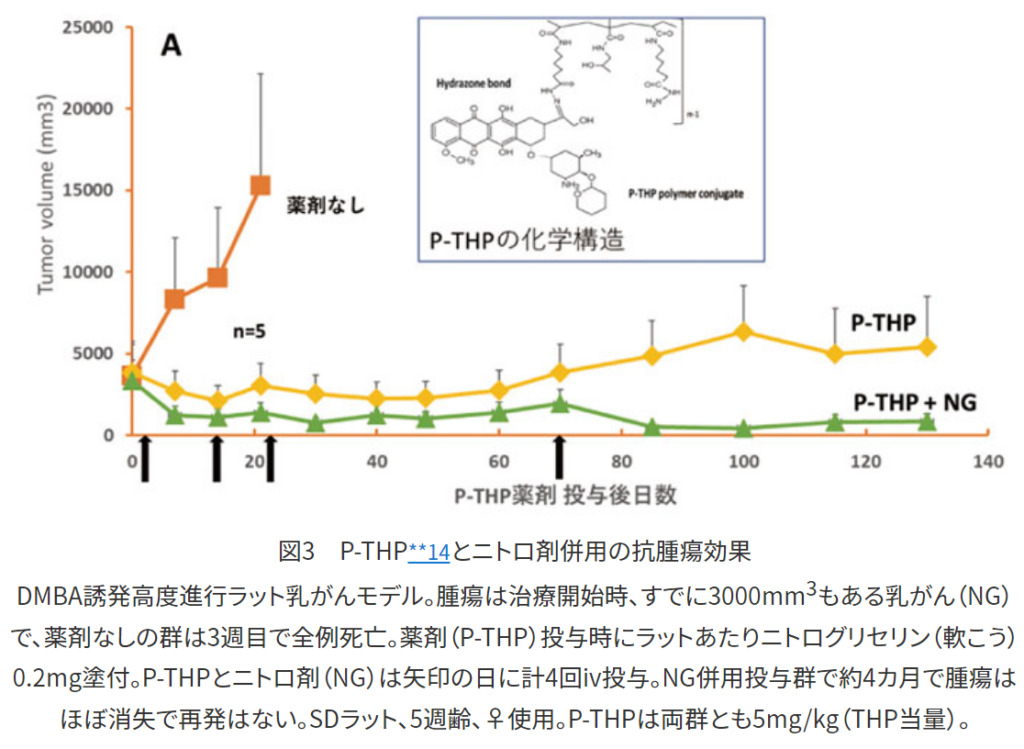
・P-TPH
⇒高分子のヒドロキシプロピルメタアクリルアミド(HPMA)ポリマー結合THP(ピラルビシン)であり
⇒その平均分子量約4万で、ヒドラゾンを介して結合している。
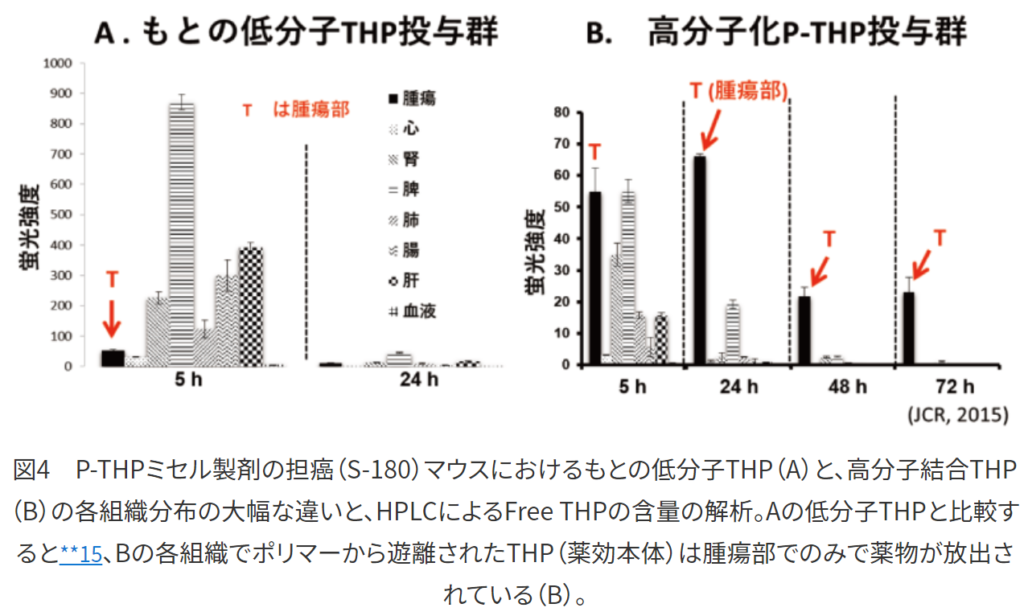
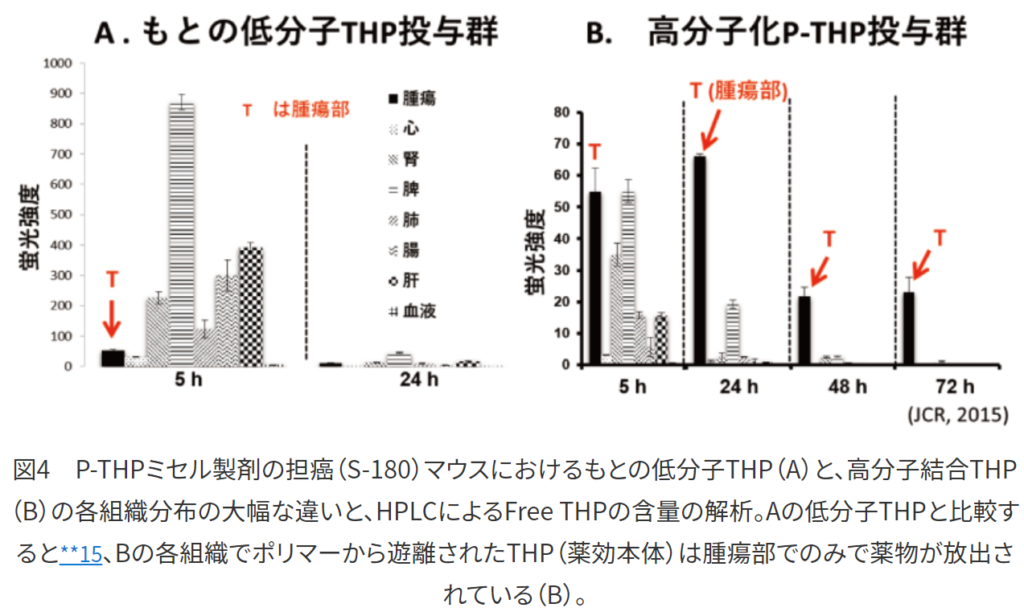
・高分子化P-THP投与群(B)
⇒Bの各組織でポリマーから遊離されたTHP(薬効本体)は腫瘍部のみで薬物が放出されている。
⇒以上のような知見に基づき、P-THPのパイロットスタディを行った。
⇒副作用がない状況で
⇒充分な抗腫瘍効果が見られた。
⇒今後の臨床が楽しみである。
■EPRに基づく実例と展望
◆EPR効果のある制癌剤(高分子化薬)
・全てで画期的な制癌効果が得られるか
⇒必ずしもそうではない。
・EPRの効果
⇒標的腫瘍までの三合目から四合目までの話で、
⇒運よく腫瘍局所に薬剤が到達したとしても、
⇒それに含有されている薬物の活性本体(API:active pharmaceutical ingredient)が癌細胞の標的に結合するかどうかである。
⇒これまで数多くのナノメディシンが開発されてきたが
⇒真に頂上まで到達した制癌剤はない。
・市販品
⇒ドキシル(ドキソルビシン含有リポソーム)やアブラキサン(アルブミン結合したタキソール)が有名である。
⇒前者は安定性が強すぎて、リポソームからのAPIの放出が遅すぎて、毒性は1/10であるが薬効はもとのドキソルビシンと変わらない。
⇒後者はこの高分子複合体からの薬物の放出が速すぎて副作用も強い。
◆P-THP(故前田 浩氏が中心に開発していた)
⇒ほぼ九合目~十合目にあると考えている。
⇒図4のBはP-THP投与後の分布図である。
⇒図2(下図)にあるようなEPR効果による腫瘍局所に選択的に集積し、
⇒腫瘍局所の低いpHでAPI(ピラルビシン、THP)を放出する。
⇒これが癌細胞に高発現しているグルコーストランスポーターなどにより、
⇒急速に細胞内へ取り込まれ
⇒その効率は
⇒同じアントラサイクリン系のドキソルビシンやエピルビシンの同じ高分子化合物よりも
⇒30~100倍も良い。
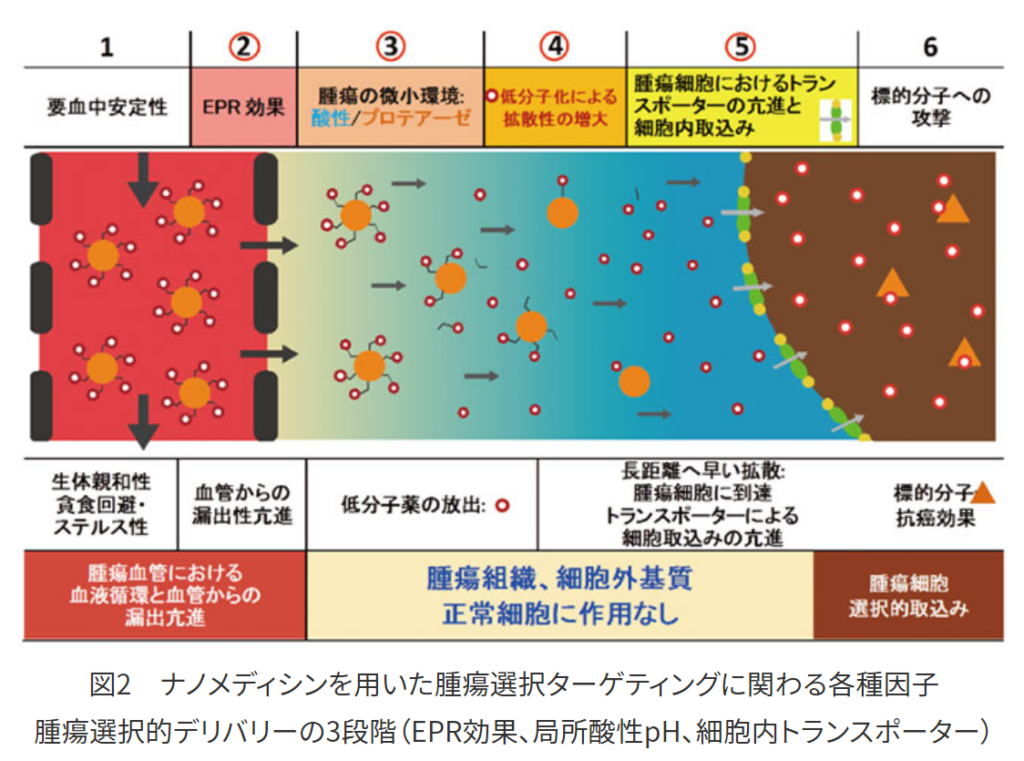
・P-THPのみスフェロイド腫瘍によく浸透する。
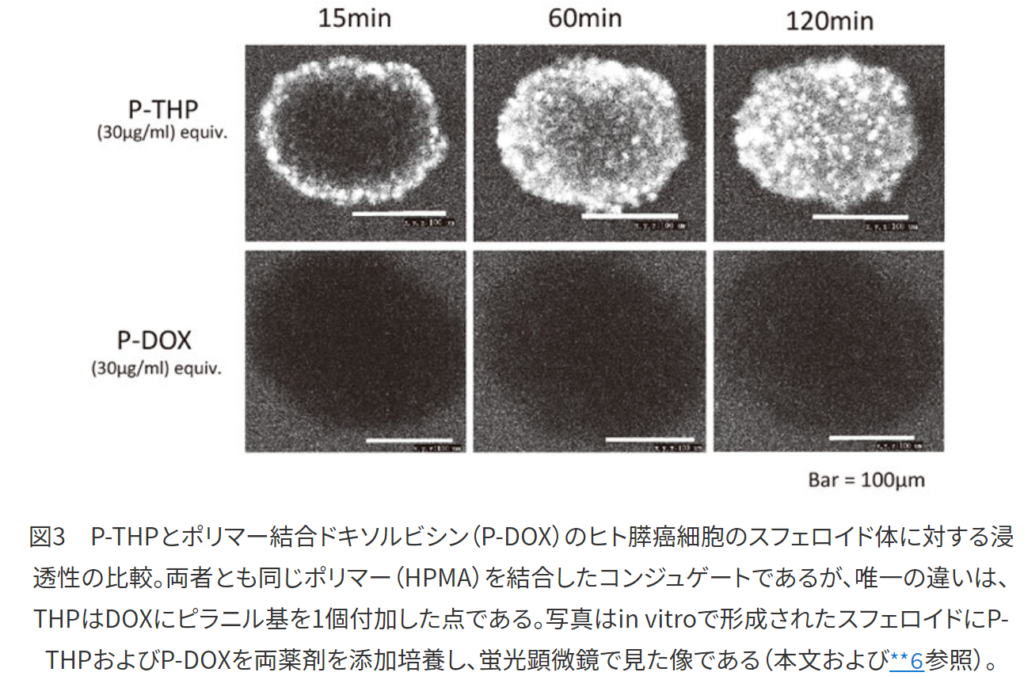
・三段階の腫瘍選択メカニズム
第一段階:EPR効果によって腫瘍に集まる(腫瘍部の新生血管の隙間から漏出する)
第二段階:腫瘍周辺の酸性pHで切れて高分子から薬剤が離れる
第三段階:グルコーストランスポーター内部に運ばれる。
正常/健常組織細胞に対する毒性は極めて低い。
このようにP-THPはまさに副作用のない、人にやさしく、かつ有効性の高い制癌剤である。
われわれとしては、このような薬剤開発に対してこそ、
公的なサポートが待たれるところである。
以上の内容は
故前田 浩氏の発表資料:高分子薬剤の切り拓くNew Dimension
─副作用のない固型癌に普遍的な制癌剤は可能だ─(1)から(4)の内容を抜粋して転記(2018年4月15日(1)、5月15日(2)、6月15日(3)、7月15日(4))
注)グルコーストランスポーターの働き例
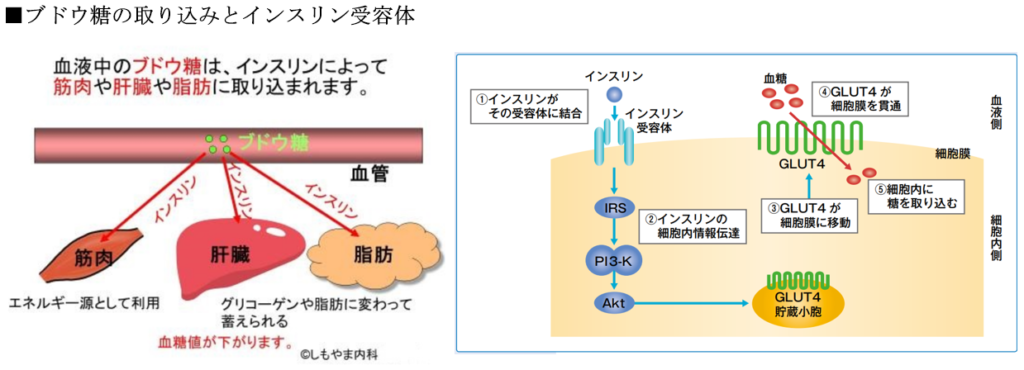
◆2020年9月20日 神戸新聞の記事(前田 浩氏へのインタビューより)
・野菜スープにコロナを防ぐ効果があるのでしょうか 宍栗出身のノーベル賞有力候補・前田浩さん(81)
⇒EPR効果のある薬の実用化はどこまで?
⇒われわれが開発した薬は臨床的な研究で副作用もなく効果を発揮したが
⇒製薬会社による治験まで進んでいない。
⇒薬の販売には効果の検証など多額の費用が必要で企業にとっても挑戦です。
⇒世の中に出るのにあと数年はかかるでしょう。
⇒同じ時期にノーベル賞候補に挙がった本庶佑先生は2018年に医学生理学賞を受賞した。毎年どんな思いでノーベル賞を見守っていますか?
⇒周りが騒いで、困ったものです。ナノ(10億分の1)テクノロジーという点で化学賞候補らいしけど、まだ5年は早いでしょう。
⇒薬が臨床で使われてくれば、みんな画期的だと分かると思う。
⇒そうなれば医学賞ですかね
◆ネット上見つけた事例
・『副作用のない抗がん剤P-THP』の前田教授からメールが来た
⇒夫の病状の概要を書いて、治療を受けさせていただけないかとのメールを送信した。
⇒その日のうちに、大学研究所名、住所、電話、FAX番号、ご本人の署名付きのメール返信が有った。
・返信内容から一部抜粋
⇒このP-THPは未承認薬のため、
⇒大学の研究室で細々と作らているのみで、
⇒供給に限りがあるため、広くお使いただくことができません。
⇒早くこの薬を世に出すべく、日々努力しておりますが、現段階ではお断りせざるを得ない状況にあります。
⇒せっかくお問合せいただいたのに、お力になれず、心苦しいのですが、どうか現状をご理解いただき、ご了承いただきたく存じます。
⇒ご主人の病状が快方に向かわれますことを心よりお祈りいたしております。
注)きんたろうの家 医療過誤★すい臓がんのブロック より転記。
■熾烈化する?「第5のがん治療」争い
ホウ素中性子捕獲療法の高分子型ミセル完成
以下のURLから転記する
https://medical-tribune.co.jp/news/2021/0220535370/index.html?_login=1#_login
光免疫療法と並んで、「第5のがん治療」と期待されるホウ素中性子捕獲療法(BNCT)。
バイオダイナミックス研究所理事長の前田浩氏(熊本大学名誉教授、東北大学特別招聘プロフェッサー)らは、
BNCTに用いるホウ素製剤の高分子化に成功したと発表した(Biomaterials 2021; 269: 120631)。
これにより、副作用を大きく減少し、より強力ながん治療が可能になるという。今年(2021年)1月に臨床応用が始まった光免疫療法(関連記事「光免疫療法がもたらす頭頸部がん治療の未来」)に注目が集まっているが、「第5のがん治療」争いが熾烈化するかもしれない。
■低分子型製剤に比べ、担がんマウスで10~20倍の抗がん作用
BNCTはホウ素と中性子線との核反応の結果生じるα線により、がん細胞を殺傷する新しいタイプの放射線療法。
外科治療、化学療法、放射線療法、免疫療法に続く第5のがん治療の1つとして、期待されている。
BNCT用のホウ素製剤としては昨年(2020年)3月、ボロファラン(10B)が世界に先駆け日本で初承認され、5月に発売されている。
BNCTでは患者にホウ素製剤を投与した上で、中性子線の照射を行うが、ホウ素製剤をいかにがん細胞に集積させるかが臨床応用の鍵であった。
ホウ素製剤が正常組織にも分布すると、中性子線照射時に正常組織にも傷害が及ぶ。
ところが、前田氏らによると、これまでBNCTに用いるホウ素製剤には低分子化合物しかなく、正常組織にもがん組織にも同様に分布することが問題であった。
同氏は1986年に、高分子型抗がん薬を静脈内投与すると通常の低分子薬剤に比べ10~50倍も腫瘍選択的に集積する現象「EPR効果(enhanced permeability and retention effect)」を発見したことで知られる
(Cancer Res 1986;46:6387-6392)。
今回、同氏らはEPR効果に基づいて、ホウ素含有の高分子型ミセル(SGB-ミセル)を開発した。SGB-ミセルは従来の低分子型ホウ素製剤と比べ、10~20倍がん局所に集中させることができる。
実際、がん細胞を用いた実験では、低分子型に比べSGB-ミセルによるBNCTはin vitroで約16倍、担がんマウスでは10~20倍の抗がん作用が認められた。
同氏らは、皮膚、造血器腫瘍など主要臓器に対する副作用は皆無であったことを強調している。
なお、SGB-ミセルは、α線によるがん細胞殺傷作用以外にも、①高度進行がんが依存しているエネルギー源である解糖系を抑制②がん細胞のミトコンドリアを障害―という新たな作用機序も併せ持つという。
■中性子線源の超小型化も実現
これまで、BNCTに用いる中性子線源には原子炉か大型加速器が想定されており、極めて高価であった。しかし最近、福島県のベンチャー企業(福島SiC応用技研)が超小型化に成功し、価格も使用電力も従来の装置の10分の1に抑制している。
前田氏らは、同社および筑波大学、神戸大学、熊本大学、大阪大学、東北大学と共同研究を始めている。同氏らは「BNCTのより広い実用化が見えてきた」と展望している。第5のがん治療の首座をめぐり、BNCTと光療法の争いが熾烈化するかもしれない。
(平田直樹)
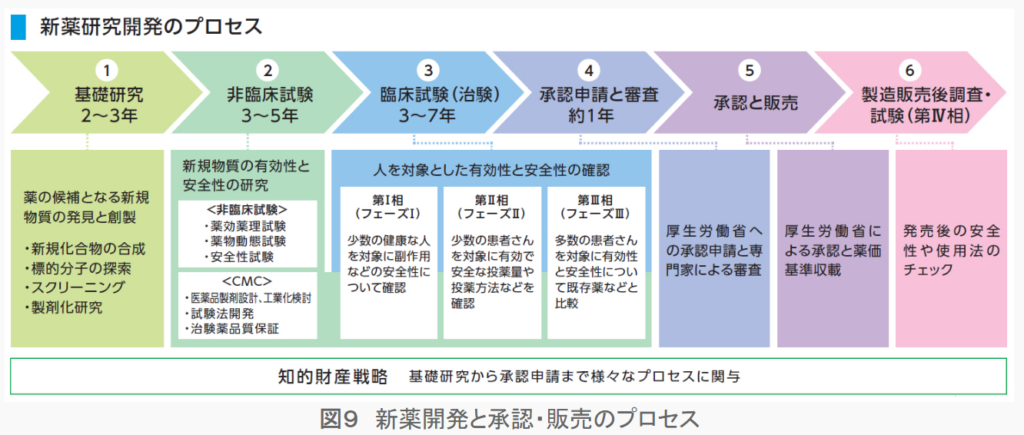
■医薬品として承認されるまでのプロセス
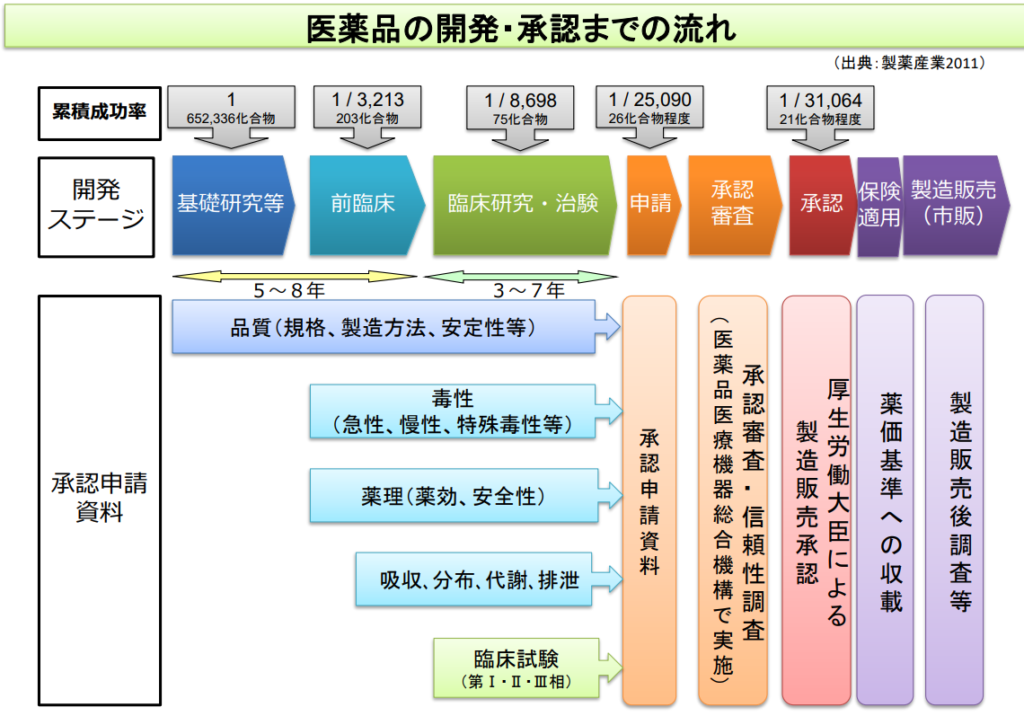
◆抗IL-6受容体抗体トシリズマブを開発した岸本軍団(元大阪大学総長 医学部)の凄さ
下記URLにて元大阪大学総長 岸本 忠三氏のインタビュー記事から一部を紹介する。
https://brh.co.jp/s_library/interview/59/
・IL-6基本メカニズムの解明の集中とIL-6受容体の探索の方針を立てる
⇒受容体の単離から、細胞内にその刺激を伝えるシグナル分子の解明まで突き進みました。
⇒最初は競争していたライバルたちも、「岸本軍団には勝てない」と次々にあきらめ、最後は独走状態でしたね。
・後に医薬品の開発を行う際も、
⇒基本的な発見についてはすべてわれわれが権利を持っていると認められ、
⇒製薬会社との共同研究も非常にスムーズにいきました。
・小規模な臨床試験で効果を確かめ
⇒基礎研究の時から共同研究をしていた中外製薬と連携して
⇒大規模な臨床試験と大量生産の技術開発をしました。
⇒このとき、IL-6関係の特許をおさえていたことがポイントだったんですよ。
・世界中で使われる薬にするための産業化は
⇒企業の役割ですが、
⇒そこに研究者が話を持ち込むには「ここまでわれわれは先行した研究を行っています」と言わなければならない。
そもそも近代医学は、北里柴三郎の血清療法、パスツールのワクチンなど免疫反応を医療に活かすことから始まりました。この長い医学の歴史の中で良い薬を生み出す近道は、基礎に徹することです。
最近の産学連携の議論では、研究をすぐに応用につなげろ、大学はビジネスのシーズを育てろと言うひとが多いのですが、「あほちゃいますか」と思いますね。流行を追っていても本質の研究がなければ特許もとれません。
自分が大事だと思うことを研究し、成果を着実に積み上げていって、最終的に役に立つことは何かと考えていけばいいのです。
「大きな種は継続した研究から生まれる。
真髄をついた研究はいつかはちゃんと役に立つんや」
と言いたいですね。
以上、インタビュー記事から一部を抜粋。
■細胞と細胞の間の二大コミュニケーション方法(IL-6シグナル伝達経路)
①細胞の直接接着
②細胞が分泌する可溶性の低分子『サイトカイン』によって担われている
・サイトカイン
⇒インターロイキン(IL)、ケモカイン、細胞増殖因子等、数百の分子が同定されている。
⇒免疫系の細胞が発現する分子群を『白血球間の信号伝達に関与する』と言う意味の名前から
⇒インターロイキン(IL)と呼んでおり、30種類以上のものが同定されている。
⇒IL-6は免疫系をコントロールしたり活性化する代表的なインターロイキンである。
◆IL-6シグナル伝達経路
・IL-6が細胞に作用するため
⇒『細胞表面上のIL-6受容体』にIL-6が結合して複合体を形成する事
⇒同上の複合体は信号伝達分子gp130に会合してgp130の2量体を誘導する事
⇒チロシンキナーゼであるJAKに結合し、これを活性化することで細胞にシグナルが伝達される。
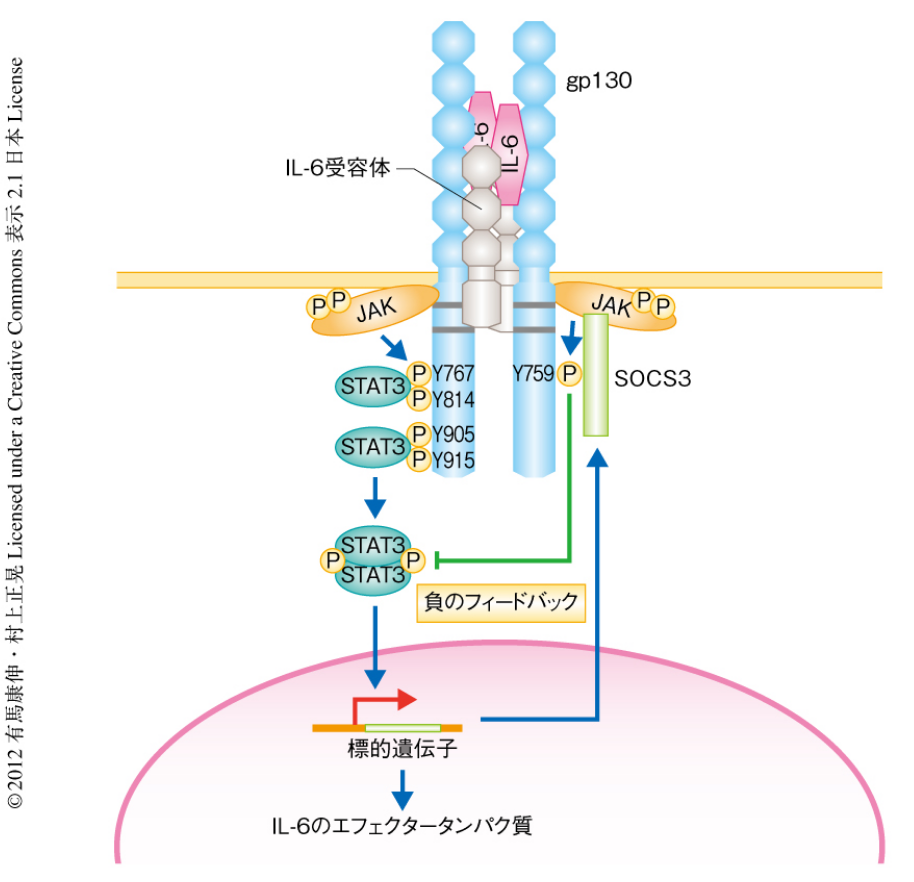
・JAKの活性化によりリン酸化されたgp130のC末端側の4つのチロシン残基
⇒Y767、Y814、Y905、Y915にはSTAT3が結合し
⇒STAT3はJAKによりさらにリン酸化されて二量体化し核へと移動する。
・STAT3の標的タンパク質であるSOCS3は
⇒JAKによりリン酸化されたgp130のチロシン残基Y759およびJAKに結合し、
⇒JAKの活性化を抑制することによりSTAT3の活性化を収束させる。
注)P:リン酸化
◆慢性関節リウマチへの大きな治療効果を解明した分子機構(IL-6アンプ)
・変異を導入したgp130を発現するマウス(F759)の実験
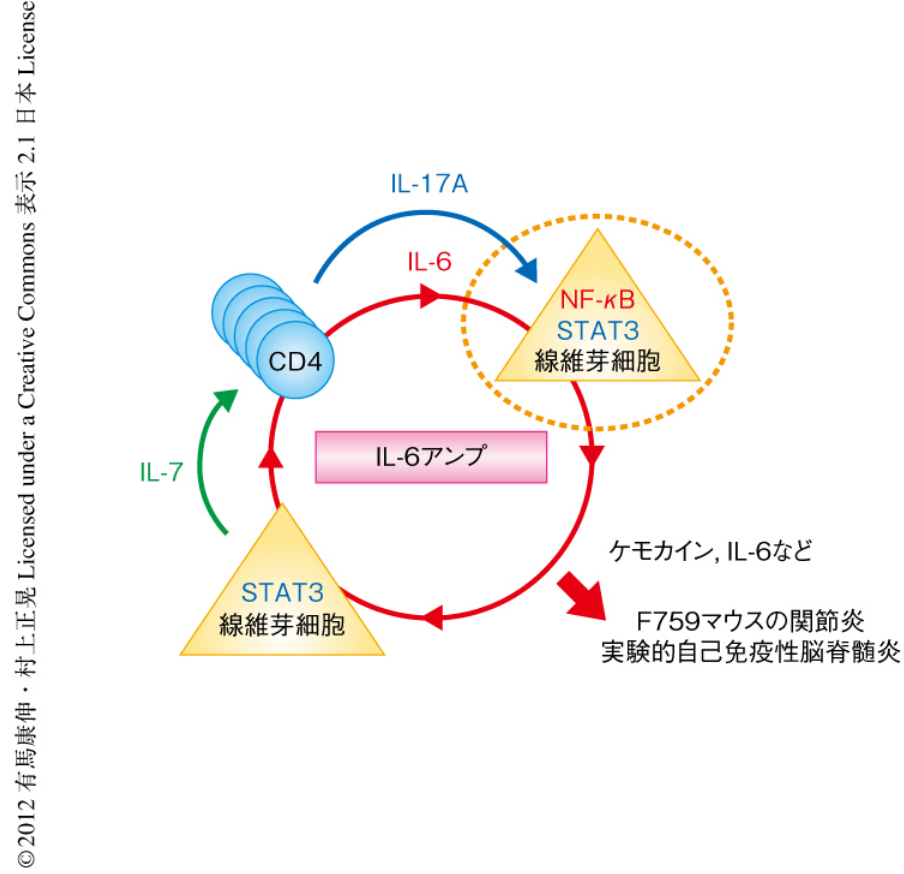
⇒関節リウマチ様関節炎を自然発症する事が明にされた。
・IL-6シグナル異常で
⇒関節リウマチ等の自己免疫疾患が発症する事を実験的に初めて明らかにされた。
・マウスの解析を通じて
⇒繊維芽細胞へのIL-6 STAT3信号の異常な活性化が
⇒IL-7を誘導して
⇒Th細胞(ヘルパーT細胞)の増加を引き起こし、病気を誘導する事
⇒更に、Th17細胞の産出するIL-7がIL-6と作用して
⇒更なIL-6産生を引き起こすIL-6増幅回路(アンプ)が存在する事が示された。
上記内容は下記URLより「インターロイキンと大阪大学」より転記
http://seisan.server-shared.com/614/614-12.pdf
■既知のがんの形成・進展過程の枠組み
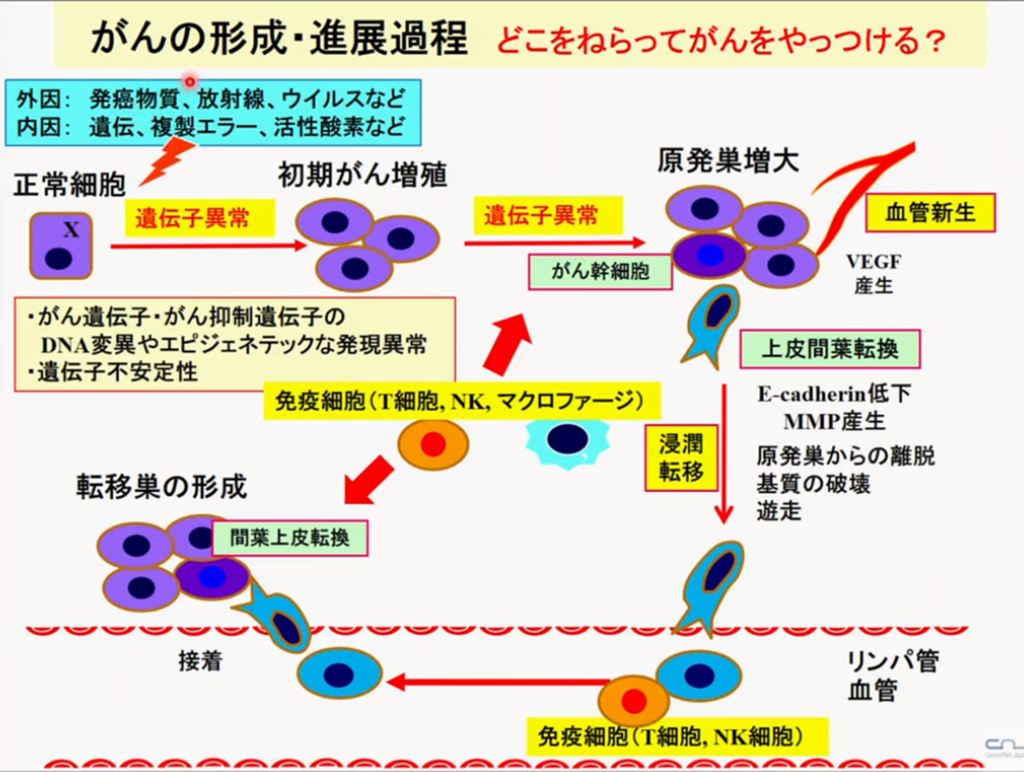
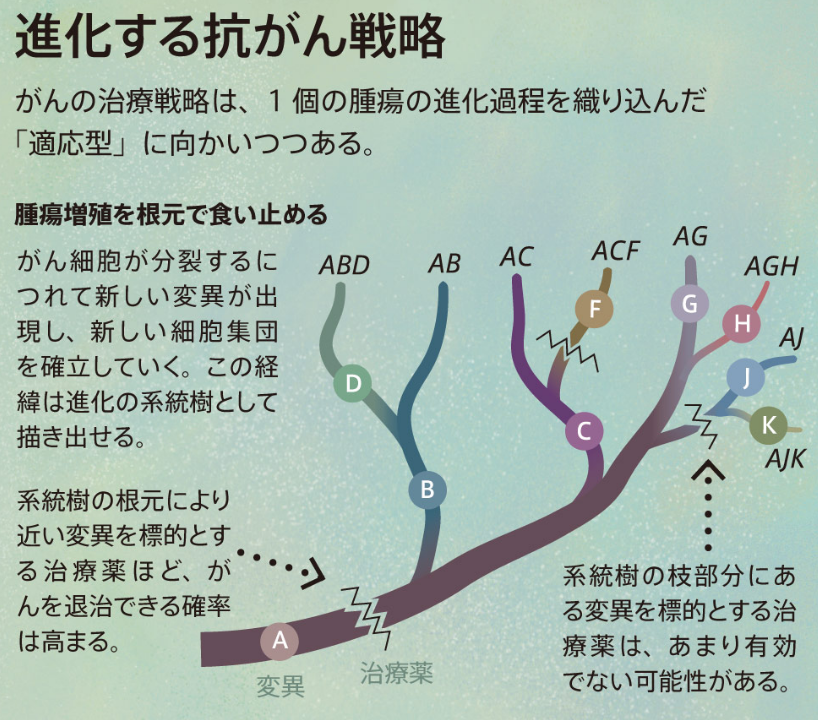
がんの進化を利用した治療戦略
■mRNA 癌ワクチンの開発動向
世界初の「がんワクチン」を開発しているのはドイツのバイオ企業「ビオンテック」です。
新型コロナウイルスのワクチンをファイザー社と共に開発したことで知られています。
・独・ビオンテック ウール・シャヒンCEO、オズレム・テュレジCMOがBBC番組での発言
⇒「私たちが『がんワクチン』開発のために何十年も研究してきたことが、
⇒新型コロナワクチン開発の追い風になりました。
⇒そして今、その開発で培った経験ががん研究に活かされています。
⇒がんの治療用ワクチンは2030年までに広く利用できるようになるでしょう」
・独・ビオンテック カタリン・カリコ上級副社長
⇒「ある種の肝臓疾患や心臓疾患の治療にもなりますし、
⇒メッセンジャーRNAがとても多くの異なる用途や他の病気に使われるようになるでしょう」
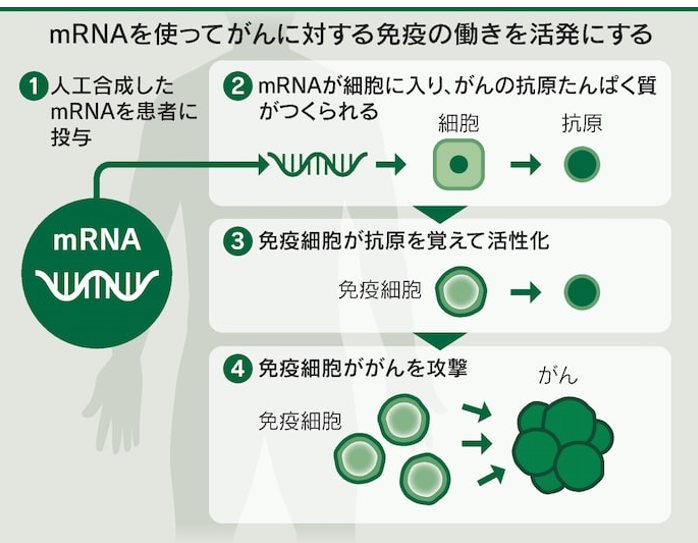
◆mRNA技術を応用
「ワクチン」といってもがんを予防するものではなく、がんを治療するためのもの。
・患者ごとにつくる「オーダーメイドワクチン」
⇒患者ごとに最も効果が期待できるように作れる。
⇒「メッセンジャーRNAというのはたんぱく質の設計図
⇒その情報の部分はいくらでも書き換えられる。
⇒ですから患者さんのがん組織を直接とって、その異常な部分を調べて、
⇒それに対するワクチンを1人1人に設計して、それをメッセンジャーRNAの形で投与する。
⇒この細胞は敵だぞ、やっつける相手だぞという風に体の免疫システムに認識させて治療に役立てる」
⇒『個別化医療』という時代(まさに21世紀にふさわしい)の幕開けを予感させる。
◆免疫療法とmRNAがんワクチンの研究
・多くの相乗効果がある。
⇒ワクチンは免疫チェックポイント阻害薬(オプジーボ等)の成功をもとに成り立っており
⇒その基礎となる生物学の知識を広げる。
・mRNAワクチンの積み荷の修飾と保護
⇒mRNAワクチンを成功させるにはmRNAを体内に送達できる技術が不可欠である。
⇒もし、mRNA配列が何の防御策もなく体内に注入されると、免疫系に異物として認識され破壊されてしまう。
◆一部の開発中のがんワクチンが採用している解決策は
①mRNAを脂質ナノ粒子(mRNA分子を保護する微小球体)で包装することである。
⇒ファイザー社/ビオンテック社のmRNA新型コロナワクチンでは、
⇒脂質ナノ粒子に封入されたmRNAが使用されている。
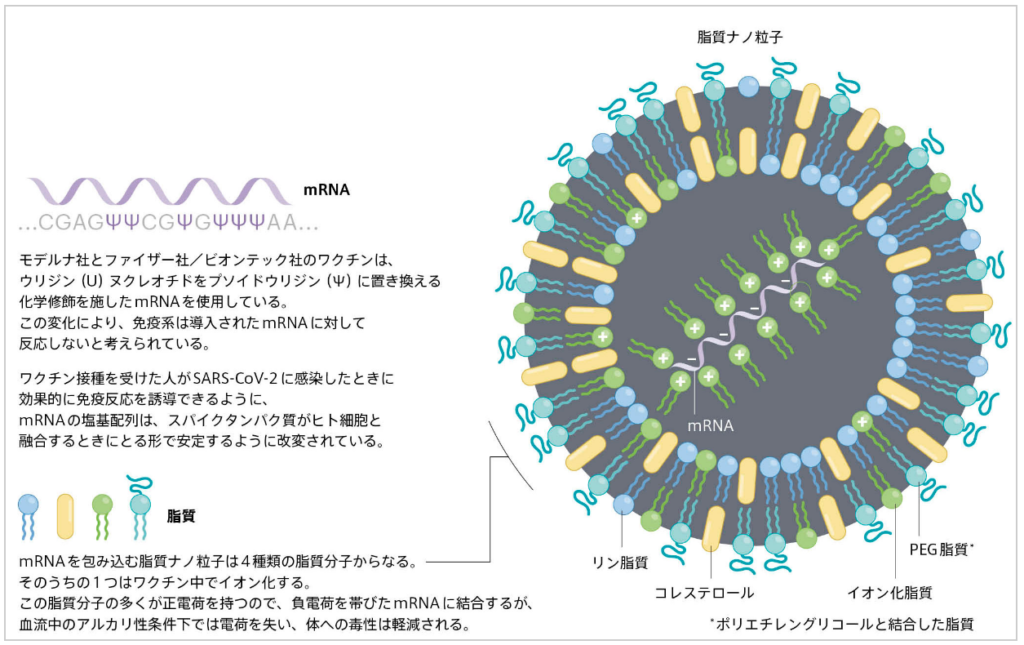
mRNAベースのCOVIDワクチンは、脂肪の泡である脂質ナノ粒子を利用して細胞内にメッセンジャーRNA(mRNA)分子を送り込む。
このmRNAには新型コロナウイルス(SARS-CoV-2)が細胞内に侵入する際使用するスパイクタンパク質の設計図がコードされていて、接種を受けた人の細胞にスパイクタンパク質を作らせる。このワクチンの設計の革新的な点を上図に示す。 出典:Nature Japan Nature ダイジェスト Vol. 18 No. 11 Feature
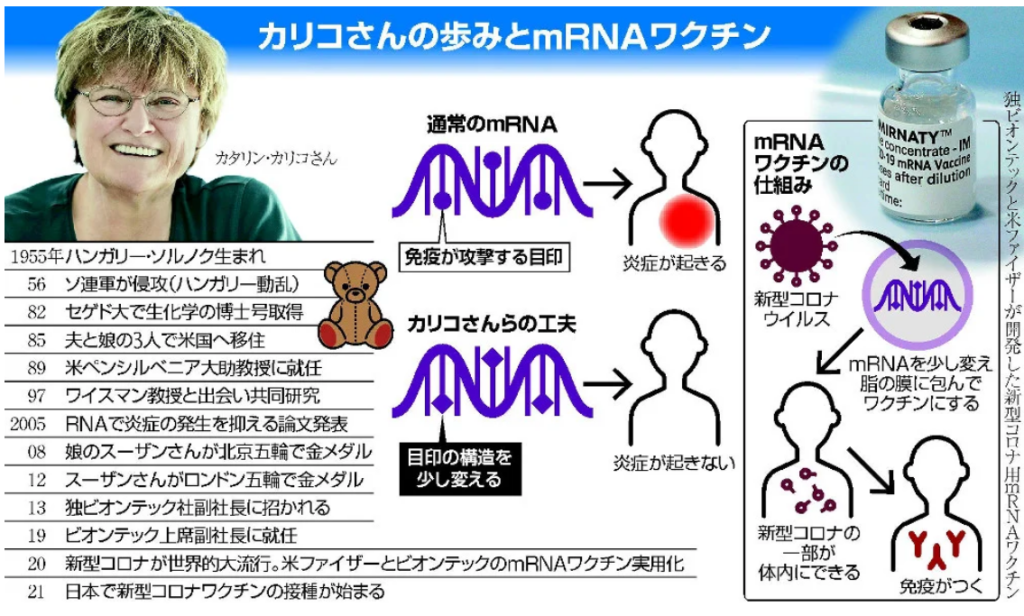
mRNAワクチン完成までの長く曲がりくねった道
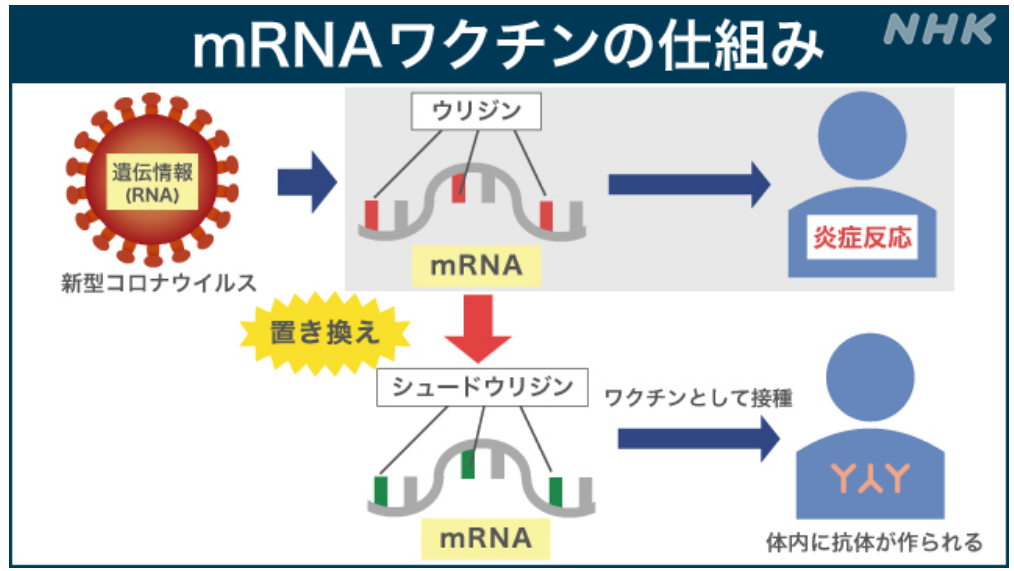
⇒もう1つの重要な特徴は、修飾型mRNAを使用している
⇒こうしたワクチンのmRNAには、シュードウリジン(天然に存在するヌクレオシドの修飾体:炎症反応を抑える物質)が組み込まれている。
⇒ヌクレオシドはmRNAの構成要素で、
⇒特定のヌクレオシドの配列によってmRNAが細胞内のタンパク質合成機構に与える指令内容が決定される。
⇒シュードウリジン修飾により、免疫系がmRNA自体をほとんど認識できなくなるようだ。
②その他の送達手段には、リポソーム(小胞、つまり泡状の物体の一種)がある。
⇒EPR効果を利用した高分子制癌剤(分子標的薬)
◆個別化mRNAがんワクチンの製造時間
・開発中のmRNAワクチンは、腫瘍の特異的な分子的特徴に基づいて個人用に製造される。
⇒患者から組織検体を採取してから、個別化mRNAがんワクチンを製造するまでに1~2カ月を要する。
・個別化がんワクチンの接種
⇒速さが特に重要です。
⇒高度に個別化された混合ワクチンの設計及び製造は
⇒腫瘍生検の実施から数週間以内に実施する必要があると
Mathias Vormehr博士(ビオンテック社がんワクチン部副部長)は述べた。
◆mRNAワクチンによる個別化された免疫療法に期待されているのは
⇒異常な分子的特徴に基づいて、
⇒個々のがん細胞を特異的に認識するT細胞を活性化できるようになること
COVID-19 mRNAワクチンの世界的な使用によって、
この手法の安全性が実証され、
がんワクチンの扉が開かれようとしている
🔶世界初!からだ自身が“がん治療” 九州大学が開発
日本人の最も多い死因「がん」。その主な治療法として知られる抗がん剤ですが、副作用があり治療を躊躇する人も少なくありません。
そんな中、九州大学が副作用もほとんどないという、世界初の治療方法を開発しました。
「ここです。細胞を扱う装置。まさにこれがマックトリガーです。
液体は栄養分でマックトリガーを優しくさすっているという状況」 こちらが、九州大学の新居輝樹助教ら研究グループが開発した細胞医薬、その名も「マックトリガー」です。
新居助教「一言でいうと、お薬ではなくてがんを生体が退治するきっかけを与えている物質。闘いのゴングを鳴らしてあげる物質」 闘いのゴングを鳴らす物質ー。
仕組みはこうです。 通常、からだにできた「がん」は、炎症を起こさず、自分が「異物」と認識されないように振る舞うため、免疫からの攻撃を受けることなく次第に成長します。
一方、新居助教らが開発した「マックトリガー」は、がんにたどり着くと炎症を引き起こすようプログラムされた細胞で、これを患者に投与します。
ひとたび、がん細胞に炎症が起きると、免疫ががんを異物と捉え、からだからの排除を試みてがんが消えていくというシステムです。
新居助教「一回投与すればあとは勝手に体ががんを治してくれる。がんがどんどん小さくなっていく」 実際に投与したマウスではがん細胞が少なくなっていることが確認されました。
その成果を最初に発見したのは研究室の学生たちでした。
九州大学大学院工学研究院・谷戸謙太さん「すごくうれしかった。すぐ報告して一緒にその喜びを分かち合ったというか」 新居助教「抱きつきましたよその時は、廊下で。こんな感じだったよね」
マックトリガーは、からだ本来が持つ排除機能を使うため、副作用はほとんどなく健康的な臓器にも影響しないのが最大の特徴です。
新居助教「これを打てば必ず治るような。しかも副作用もなく自分自身のパワーによって直せるから安心な治療ができるというところで、世界を変えることができるかなと」 実用化が待たれるところですが、臨床実験などを重ねる必要があり「あと10年以上かかるのでは」ということです。